
A、 N2(g)+3H2?2NH3(g)△H<0 |
B、 FeCl3+3KSCN?Fe(SCN)3+3KCl |
C、 向稀醋酸中加入醋酸钠溶液 |
D、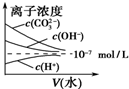 稀释苏打溶液 |


科目:高中化学 来源: 题型:
| A、二氧化硫可用于纸浆漂白,表明二氧化硫具有还原性 |
| B、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| C、明矾可用于净水是因为它能够消毒杀菌 |
| D、静电除尘、血液透析均与胶体性质相关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精能使蛋白质变性,可用于杀菌消毒 |
| B、CaO能用于燃煤的脱硫 |
| C、明矾水解时产生具有吸附性的胶体粒子,可以除去水中的杂质离子 |
| D、氯气泄露时,人群应向高处疏散 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)
N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )
N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )| A、减小NO2的浓度 |
| B、降低温度 |
| C、增加压强 |
| D、升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第一电离能:③>①>② |
| B、原子半径:③>②>① |
| C、电负性:③>①>② |
| D、最高正化合价:③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 压强(MPa) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 氨的平衡含量(%) | ||||||
| 温度(摄氏度) | ||||||
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.1 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验序号 | 盐酸体积/ml | NaOH溶液体积/ml |
| 1 | 25.25 | 25.00 |
| 2 | 25.23 | 25.00 |
| 3 | 25.27 | 25.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中所有碳原子在同一直线上 |
| B、分子中所有氢原子一定在同一平面内 |
| C、分子中在同一平面内的原子最多有6个 |
| D、分子中在同一平面内的原子最多有9个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com