
下列离子或分子组中,在相应的环境中能大量共存的是( )
选项 | 环境要求 | 离子 |
A | 溶液中c(K+)<c(Cl-) | K+、AlO2-、Cl-、NO3- |
B | 溶液pH﹥7 | Na+、S2-、K+、ClO- |
C | 水电离产生的c(H+)=10-12 mol/L的溶液 | ClO-、CO32-、NH4+、NO3-、SO32- |
D | 向溶液中逐滴滴加烧碱溶液先有沉淀产生,后沉淀消失 | Na+、Al3+、Cl-、SO42- |
科目:高中化学 来源:2016届山东省高三12月月考化学试卷(解析版) 题型:选择题
下表中的事实与推论不符的是( )
序号 | 事实 | 推论 |
A | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
B | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
C | SO2与NaHCO3溶液反应生成CO2 | 非金属性:S>C |
D | HCl热稳定性比H2S强 | 非金属性:Cl>S |
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期期中联考化学试卷(解析版) 题型:推断题
I:A、B、C、D均为中学化学中常见的物质,它们之间转化关系如下图(部分产物已略去):

试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为___________(填元素符号)
(2)若D是金属,C溶液在储存时应加人少量D,其理由是(用必要的文字和离子方程式表示)_______________________.
(3)若A、B、C为含同一种金属元素的无机化合物.在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式_______________________。
化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E的混合物投人500m1稀硫酸中,固体全部溶解并产生气体。待反应完全后.向所得溶液中加人NaOH溶液,生成沉淀的物质的是与加入溶液的体积关系如下图所示:
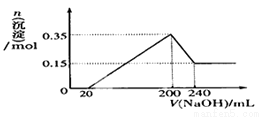
则固体混合物中Mg的质量为_____________;NaOH溶液的物质的量浓度为___________。
II某一离子反应体系有反应物和产物共以下六种:MnO4—、H+、O2、H2O、H2O2、Mn2+。已知该反应中的H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是___________。
(2)该反应中.发生还原反应的过程是_____→_____。
(3)溶液随着酸性的增强氧化性不断增强,应选择__________(选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(4)如反应转移了0.6mo1电子,则产生的气体在标准状况下体积为__________。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:选择题
下列叙述正确的是
A、稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B、25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7]
C、25℃时,0. 1mo1·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D、0.1 mol AgCl和0. lmo1 AgI混合后加入1L水中所得溶液c(Cl-)=c(I-)
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三上学期统练(三)化学试卷(解析版) 题型:选择题
在298 K、101.325 kPa时发生下列反应:①2H2(g)+O2(g)=2H2O(l) ②CaO(s)+CO2(g)=CaCO3(s);其熵变分别为ΔS1和ΔS2,则下列情况中正确的是
A.ΔS1>0,ΔS2>0 B.ΔS1<0,ΔS2<0
C.ΔS1<0,ΔS2>0 D.ΔS1>0,ΔS2<0
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第四次考试化学试卷(解析版) 题型:选择题
主族元素X在周期表中位于第二周期,其原子最外层电子数大于4,元素Y在周期表中位于第三周期,其原子最外层电子数小于4,有关其说法正确的是( )
A.X所形成的单质都是双原子分子
B.原子半径X>Y
C.X、Y能形成的阴、阳离子数之比为1:2离子化合物,其一定为碱性氧化物
D.由X、Y组成的某化合物与水反应能生成一种强碱和一种弱碱,其简单离子半径:X>Y
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:选择题
根据下图海水综合利用的工业流程图,判断下列说法不正确的是
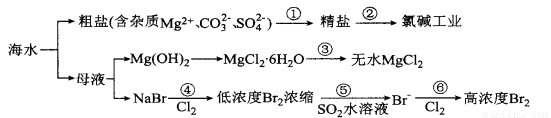
已知:MgCl2·6H2O受热生成Mg(OH) Cl和HC1气体等。
A.过程①的提纯是化学过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2·6H2O直接灼烧得不到MgCl2
C.在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:选择题
将足量的CO2不断通入KOH、Ca(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
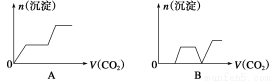

查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高级中学高三上学期期中考试化学试卷(解析版) 题型:填空题
氮是一种重要的非金属元素,可以形成多种不同类型的化合物,请根据要求回答下列问题:
(1)已知NA表示阿伏加德罗常数,在69g NO2和N2O4的混合气体中含有____NA个氧原子;在2L 0.6 mol/LFe(NO3)3溶液中含_____NA个NO3-离子。
(2)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,
①写出该反应的化学方程式 .若反应中生成0.15 mol HNO3,则该反应中转移的电子数目为 个。
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F;据题意推测 NF3, F2, NO这三种气体中,氧化性由强到弱的顺序为 。
(3)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2:1,写出该反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com