
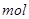 电子,则氧化产物的质量是____。
电子,则氧化产物的质量是____。科目:高中化学 来源:不详 题型:单选题
| A.阳离子只有氧化性,阴离子只有还原性 |
| B.失电子难的原子获得电子的能力一定强 |
| C.得到电子越多的氧化剂,其氧化性就越强 |
| D.要实现Fe2+→ Fe3+的转化,必须加入氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是 ,氧化产物是 ;若有1mol KMnO4参加反应时,该反应转移电子的个数是 ;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为 mol;请在下面方框中用“单线桥法”表示该反应中电子转移的方向和数目。
2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是 ,氧化产物是 ;若有1mol KMnO4参加反应时,该反应转移电子的个数是 ;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为 mol;请在下面方框中用“单线桥法”表示该反应中电子转移的方向和数目。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 3Fe+4CO2的反应中, 是氧化剂,
3Fe+4CO2的反应中, 是氧化剂,查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质间的置换反应 | B.气态氢化物的稳定性 |
| C.单质在水中的溶解度的大小 | D.最高价氧化物对应水化物的酸性强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com