
下列实验装置设计正确,且能达到目的是()
A. 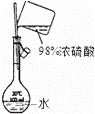
配制稀硫酸溶液
B. 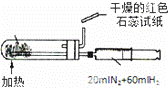
合成氨并检验氨的生成
C. 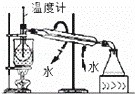
碘的CCl4溶液中分离I2并收回CCl4
D. 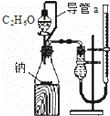
测定乙醇分子结构
考点: 化学实验方案 的评价.
的评价.
专题: 实验评价题.
分析: A.容量瓶不能用来直接稀释和配制溶液;
B.干燥的氨气不能使试纸变色;
C.温度计应测定蒸气的温度,其位置错误;
D.利用生成气体的体积确定乙醇中﹣OH,从而确定结构式.
解答: 解:A.容量瓶不能用来直接稀释和配制溶液,应在小烧杯中稀释,故A错误;
B.在催化剂的作用下生成的氨气为干燥的气体,干燥的氨气不能使试纸变色,则不能说明氨气的生成,故B错误;
C.温度计应测定蒸气的温度,其位置应在蒸馏烧瓶的支管口处,故C错误;
D.钠与乙醇反应生成氢气,利用生成气体的体积确定乙醇中﹣OH,从而确定结构式,故D正确.
故选D.
点评: 本题考查实验方案的评价,涉及溶液的配制、气体的检验、物质的分离、结构式的确定,注重对实验中的操作的考查,题目难度不大.


科目:高中化学 来源: 题型:
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别是b mol·L-1和2b mol·L-1,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用 ( )。
A.Ca(OH)2 B.NaOH
C.NaHCO3 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
“类推”的思维方式在化学学习与研究中经常采用,但有时会产生错误结论.下列类推结论中,正确的是()
A. 由氢氟酸刻蚀玻璃可推知盐酸也能用来刻蚀玻璃
B. 由Na2O中阴阳离子个数比为1:2,可推出Na2O2中阴阳离子个数比为 1:1
C. 由钠与冷水剧烈反应,可推知钾也能与冷水剧烈反应
D. 由“2Fe+3Br2═2FeBr3”反应可推出“2Fe+3I2═2FeI3”反应也能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
将Fe(OH)3胶体与BaCl2的混合液装在半透膜中,浸泡在装有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是()
A. 溶液为黄色
B. 能产生丁达尔效应
C. 加入AgNO3 溶液产生白色沉淀
D. 加入Na2SO4 溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
NO2通过盛有水的洗气瓶,转移0.02mol电子时,参加反应的NO2气体在标准状况下的体积为()
A. 224mL B. 336mL C. 448mL D. 672mL
查看答案和解析>>
科目:高中化学 来源: 题型:
由A、B两种粉末组成的混合物,在一定条件能发生如图所示的转化关系.其中B、C均为氧化物,J为黄绿色气体,部分反应产物已略去.
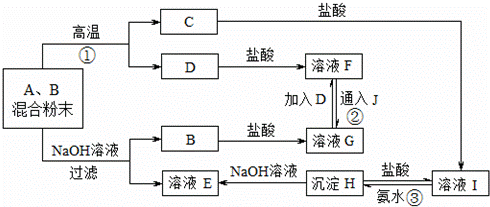
请 回答:
回答:
(1)写出相应物质的化学式:A ,B
(2)写出图中相应转化的离子方程式:反应② 反应③ (3)反应①的主要用途是 (回答一条即可).
(4)以下选项中的试剂可以检验溶液F中的金属阳离子的是 (填字母编号).
a.NaOH溶液 b.KSCN溶液 c.稀硫酸 d.新制氯水与KSCN溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列说法中不正确的是()
A. 一定量的Fe与含1molHNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
B. 1molFeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C. 0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA
D. 125gCuSO4•5H2O晶体中含有0.5NA个Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究SO2气体还原Fe,I2,他们使用的药品和装置如如所示.
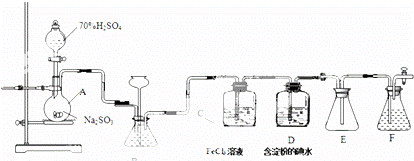
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则整个装置气密性良好.装置E的作用是 .装置F中为NaOH溶液.
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 .
a.蒸馏水
b.饱和Na2SO3溶液
c.饱和NaHSO3溶液
d.饱和NaHCO3溶液
(3)SO2气体还原Fe3+反应的产物是 (填离子符号).
(4)在上述装置中通入过量的SO2为了验证C中SO2与Fe3+发生了氧化还原反应,他们取C中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去.
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的是方案①,原因是 .
(5)能表明I﹣的还原性弱于SO2的现象是 ,写出有关离子方程式: ﹣.
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,
(1))请写出NO2和CO反应的热 化学方程式: 已知:N2 (g)+2NO2 (g)⇌4NO(g)△H=+292.3kJ•mol﹣1,
化学方程式: 已知:N2 (g)+2NO2 (g)⇌4NO(g)△H=+292.3kJ•mol﹣1,
则反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g) 的△H= ;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生反应:4NO2(g)+O2(g)⇌2N2O5(g);已知体系中n(NO2)随时间变化如表:
t(s) 0 500 1000 1500
N(NO2)(mol) 20 13.96 10.08 10.08
写出该反应的平衡常数表达式:K= ,
已知:K3000C>K3500C,则该反应是 反应(填“放热”或“吸热”).

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com