
已知A、B、C、D、E、F、G和X八种物质存在如下图所示的转化关系。其中C是过渡元素的单质,其他元素均是短周期元素;B的浓溶液和稀溶液都能与C反应,但还原产物不同;反应⑤用于传统制镜工业,X是医疗上病人重要的营养补给物质(通过输液);F是大气污染物,也是汽车尾气的成分之一。请回答下列问题:(部分生成物未标出)
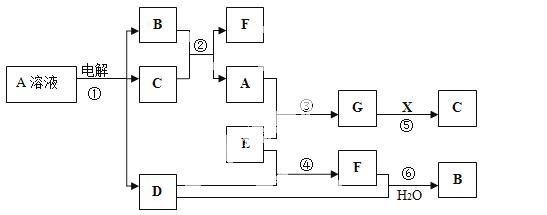
(1)A、X的化学式分别是 , ;G溶液俗称为 。
(2)写出反应①的离子方程式 。
(3)写 出E的分子式 ,请用电离方程式解释E的水溶液呈碱性的原因
出E的分子式 ,请用电离方程式解释E的水溶液呈碱性的原因
。
(4)已知1gE与足量的空气混合,在加热及有催化剂存在下发生反应生成气态产物,放出热量13.3kJ,请写出该反应的热化学方程式 。
(5)为了消除F对大气的污染,工业上采用在催化剂作用下E与F反应,将其转化为无毒气体和水,请写出该反应的化学方程式 。
科目:高中化学 来源: 题型:
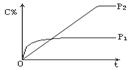
在温度相同,压强分别为p1、p2条件下,A(g)+2B(g)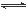 nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.
nC(g)的反应体系中,C的体积分数(C%)随时间(t)变化的曲线如图所示.
下列结论正确的是
A.p1 > p2 n < 3 B.p1 < p2 n > 3
C.p1 < p2 n = 3 D.p1 > p2 n > 3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.同主族非金属元素的简单阴离子的还原性越强,其元素非金属性越强
B.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
C.元素原子的最外层电子数等于元素的最高化合价
D.全部由非金属元素组成的化合物中只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
碳和氮的许多化合物在工农业生产和生活中有重要的作用。
(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g) === NH2CO2NH4(s) ∆H=-159.5 kJ·mol-1
②NH2CO2NH4(s) === CO(NH2)2(s)+H2O(g) ∆H=+116.5 kJ·mol-1
③H2O(l) === H2O(g) ∆H=+44.0 kJ·mol-1
则反应2NH3(g)+CO2(g) === CO(NH2)2(s)+H2O(l)的∆H= kJ·mol-1
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2 (g) ∆H=Q kJ·mol-1。
N2(g)+CO2 (g) ∆H=Q kJ·mol-1。
在T1℃时,反应进行到同时间测得各物质的浓度如下;30min后,只改变某一条件,反应重新达到平衡,各物质浓度如图所。
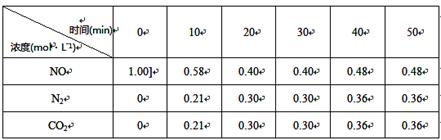
①0~10min内,NO的平均反应速率v(NO)= ,
T1℃时,该反应的平衡常数K= ;
②30min后,只改变某一条件,反应重新达到平衡,各物质浓度如图所示。根据上表中的数据判断改变的条件可能是 (填字母编号)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂 e.升高温度
③30min后,如果将温度升高至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则 Q 0(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。
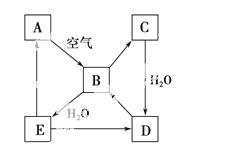
(1)写出A在加热条件下与H2反应的化学方程式:
_________________________________________________________________;
(2)写出E与A的氢化物反应生成A的化学方程式:
_________________________________________________________________;
(3)写出一个由D生成B的化学方程式:
________________________________________________________________;
(4)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式: _________________________________________;
②反应后溶液的pH________7(填“大于”“小于”或“等于”),理由是______________________________________________________________ ___;
___;
③加热反应后的溶液,其pH________(填“增大”“不变”或“减小”),理由是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。
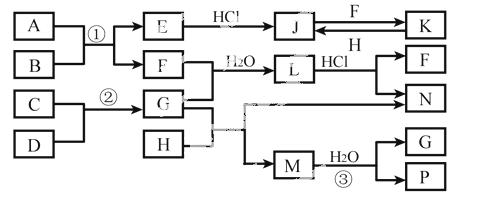
已知:E为红棕色固体,K为浅绿色溶液;反应①、②都是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F、P 和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为四原子10电子分子,化合物M由两种元素组成,分子内共有58个电子。
(1)写出F的化学式 、P的电子式 ;
(2)在G的水溶液中,阳离子浓度最大的是 (用离子符号表示)
(3)写出K与H反应的离子方程式 ;G与H反应的化学方程式
(4)在实验室中,向饱和H水溶液中加入CaCO3粉末,充分反应后过滤,可制得浓度较大的P的水溶液。用化学平衡移动的原理加以解释 。
查看答案和解析>>
科目:高中化学 来源: 题型:
嫦娥二号月球探测器获得了7 m分辨率全月球影像图,该月球探测器使用钚元素的同位素电池来提供稳定、持久的能源。下列关于 Pu的说法正确的是( )
Pu的说法正确的是( )
A. Pu和
Pu和 Pu的质子数之差为2
Pu的质子数之差为2
B. Pu和
Pu和 Pu是两种不同的核素
Pu是两种不同的核素
C. Pu的中子数与质子数之差为144
Pu的中子数与质子数之差为144
D. Pu和
Pu和 Pu互为同素
Pu互为同素 异形体
异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是
| X | Y | ||
| Z | W | Q |
A.钠与W可能形成Na2W2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q强
D.X有多种同素异形体,而Y不存在同素异形体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com