
| A�� | ʵ�������Ƶ���������Һ�ڿ����б�������4Fe2++O2+2H2O�T4Fe3++4OH- | |
| B�� | �Խ�����Ϊ������ⱥ������ͭ��Һ��Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+O2��+4H+ | |
| C�� | Ca��ClO��2��Һ��ͨ�������SO2���壺ClO-+SO2+H2O�THClO+HSO3- | |
| D�� | ���ữ�ĸ��������Һ����˫��ˮ��2 MnO4-+6H++5H2O2�T2Mn2++5O2��+8H2O |
���� A��ʵ��������������ʱ������Ӧ���������������ӵ�ˮ�⣬��Һ�����ԣ�Ӧ����ˮ��������������
B�����������ǽϻ��õĽ������������ڵ�����������ʧ���ӣ�������ͭ���ӵõ��ӣ�
C����������ǿ�����ԣ�������������������������
D�����������˫��ˮ��������������������ԭΪ���������ӣ�
��� �⣺A��ʵ��������������ʱ������Ӧ���������������ӵ�ˮ�⣬��Һ�����ԣ��������ӱ����������������ӵ����ӷ���ʽΪ��4Fe2++O2+4H+�T4Fe3++2H2O����A����
B�����������ǽϻ��õĽ������ڵ�����������ʧ���ӣ�����ʱ�����ĵ缫��Ӧ��2Ag-2e-=2Ag+�������ĵ缫��Ӧ��Cu2++2e-=Cu�������ܷ�Ӧ��2Ag+Cu2+=2Ag++Cu����B����
C��Ca��ClO��2��Һ��ͨ�������SO2��������ӷ�ӦΪ��Ca2++2ClO-+2H2O+2SO2=CaSO4��+4H++2Cl-+SO42-����C����
D�����������˫��ˮ��������������������ԭΪ���������ӣ���Ӧ���ӷ���ʽΪ��2MnO4-+6H++5H2O2�T2Mn2++5O2��+8H2O����D��ȷ��
��ѡD��
���� ���⿼�����ӷ�Ӧ����ʽ��д�������жϣ�Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ�������������ԭ��Ӧ�������йص����ӷ�Ӧ���飬ע�����ӷ�Ӧ�б�����ѧʽ�����ʼ����ӡ�����غ㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����CO2��NO��SO2��H2O | B�� | �NaOH��KOH��Ba��OH��2��Na2CO3 | ||
| C�� | ��Σ�NH4Cl��NH4NO3��NH3•H2O | D�� | ���������Na2O��CaO��CO2��Al2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{a}{14}$ mol-1 | B�� | $\frac{a}{28}$ mol-1 | C�� | 14a mol-1 | D�� | 28a mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al2O3���岻������������ˮ������Al2O3���ǵ���� | |
| B�� | Na2SO4��Һ���磬����Na2SO4�ǵ���� | |
| C�� | ������������磬��������ǵ���� | |
| D�� | 1.5mol/L��NaCl��Һ��1.0mol/L��MgCl2��Һ��Ƚϣ�������������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
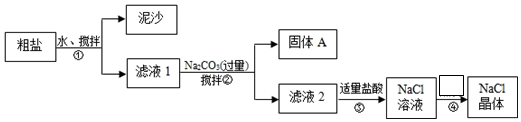
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
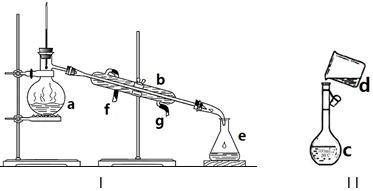
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com