
 短周期元素Q、R、T、W、Z在元素周期表中的位置如图所示,其中T是该周期离子半径最小的元素,下列说法中不正确的是( )
短周期元素Q、R、T、W、Z在元素周期表中的位置如图所示,其中T是该周期离子半径最小的元素,下列说法中不正确的是( )| A. | Q、Z、W可形成三原子直线型分子 | |
| B. | Z、R两元素气态氢化物的沸点:R>Z | |
| C. | Z、Q两元素的气态氢化物中键能大小:Z>Q | |
| D. | T、W两元素组成的化合物不能通过水溶液中的离子反应制取 |
分析 根据短周期元素Q、R、T、W、Z在元素周期表中的位置可知,Q、Z位于第二周期,T、R、W位于第三周期,T是该周期离子半径最小的元素,T应该是第三周期元素中原子序数最大的金属元素,是Al元素;根据Q、Z、R、W与T的相对位置可知R为P元素、W为S元素、Q为C元素、Z为O元素,然后结合元素周期律知识进行解答.
解答 解:根据短周期元素Q、R、T、W、Z在元素周期表中的位置可知,Q、Z位于第二周期,T、R、W位于第三周期,T是该周期离子半径最小的元素,T应该是第三周期元素中原子序数最大的金属元素,是Al元素;根据Q、Z、R、W与T的相对位置可知R为P元素、W为S元素、Q为C元素、Z为O元素,
A.W为S元素、Q为C元素、Z为O元素,三种元素可形成结构式为S=C=O的化合物,为直线型结构,故A正确;
B.Z、R分别为O、P元素,其氢化物分别为水和磷化氢,由于水分子间存在氢键,则水的沸点大于磷化氢,及两元素气态氢化物的沸点:R<Z,故B错误;
C.Z、Q两元素分别为O、C,其对应的氢化物分别为水和甲烷,非金属性O>C,氢化物稳定性H2O>CH4,稳定性越强,则键能越大,所以二者的气态氢化物中键能大小:为Z>Q,故C正确;
D.T、W分别为Al、S,两元素组成的化合物为Al2S3,由于铝离子和硫离子在溶液中发生双水解反应,所以不能通过水溶液中的离子反应制取Al2S3,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,正确推断各元素名称为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.


科目:高中化学 来源: 题型:解答题
 $→_{②Zn/H_{2}O}^{①O_{3}}$R-CHO+
$→_{②Zn/H_{2}O}^{①O_{3}}$R-CHO+
 +H2O→R-COOH+HX
+H2O→R-COOH+HX
 、
、 ;
;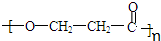 +nH2O.
+nH2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCl2=Ca2++Cl2? | B. | Na2SO4=Na++SO42- | ||
| C. | HNO3=H++NO3- | D. | NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 木炭在空气中燃烧发白光、放热 | |
| B. | 氧化反应是指物质与氧气发生的化合反应 | |
| C. | 凡是在空气中不能燃烧的物质,在纯氧中也不能燃烧 | |
| D. | 蜡烛燃烧、食物腐败都是氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知可逆反应A(g)+B(g)?C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题:
已知可逆反应A(g)+B(g)?C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
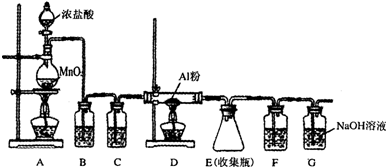
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第八周期ⅢA族 | B. | 第六周期ⅤA族 | C. | 第七周期ⅣB族 | D. | 第七周期ⅣA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCOOCH2CH2CH3 | B. | CH3CH2COOCH3 | C. | CH3COOCH2CH3 | D. | HCOOCH(CH3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com