
【题目】实验室从海带中提取碘的流程如下:
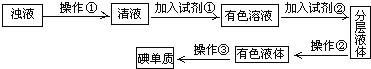
(1)指出过程中有关的实验操作①和②名称:①_______,②_______。
(2)下列物质中,能使湿润的KI-淀粉试纸变蓝的是________。
A.碘蒸气 B.Cl2 C.KI溶液 D.饱和氯化钠溶液
(3)试剂①若用氯水,请写出发生反应的离子方程式___________________。
【答案】过滤 分液 AB Cl2 +2I- =I2+2Cl-
【解析】
浊液转化为清液,采用的分离方法为过滤;将清液中I-氧化为I2,得到有色溶液,需加入强氧化剂(如氯水、双氧化水等);加入萃取剂后静置,液体分层,分液后得有色液体;再蒸馏,便可获得碘单质。
(1)从上面分析可以得出,过程中有关的实验操作①和②名称分别为:①过滤,②分液。答案为:过滤;分液;
(2)A.碘蒸气本身为I2,能使淀粉变蓝,A符合题意;
B.Cl2能与KI发生置换反应,生成I2和KCl,I2能使淀粉变蓝,B符合题意;
C.KI溶液中的I-,不能使淀粉变蓝,C不符合题意;
D.饱和氯化钠溶液不能将I-氧化为I2,不能使淀粉变蓝,D不符合题意;
故选AB。答案为:AB;
(3)试剂①若用氯水,则与KI发生置换反应,生成KCl和I2,发生反应的离子方程式Cl2 +2I- =I2+2Cl-。答案为:Cl2 +2I- =I2+2Cl-。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】浩瀚的海洋中蕴藏着丰富的资源。

(1)粗盐精制。
过程1除去粗盐中的Ca2+、Mg2+、![]() 杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液,过滤除去沉淀,再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液,过滤除去沉淀,再加入适量的盐酸。
①加入沉淀剂的顺序正确的是______(填序号)。
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有2H++![]() =H2O+CO2↑和______。
=H2O+CO2↑和______。
(2)海水提镁。
过程2中加入的试剂是______。由无水MgCl2获得Mg的化学方程式是______。
(3)海水提溴。
主要工业生产流程如图所示:

①海水中的Br-被Cl2氧化的离子方程式是______。
②吸收塔中SO2将Br2转化为HBr的化学方程式是______。
③工业上也可用Na2CO3溶液吸收吹出的Br2。补全以下化学方程式:___Br2+___Na2CO3+3H2O![]() ___NaBr+___NaBrO3+___NaHCO3,____________
___NaBr+___NaBrO3+___NaHCO3,____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
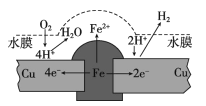
A. 腐蚀过程中铜极上始终只发生: 2H++2e-= H2↑
B. 若水膜中溶有食盐将加快铁铆钉的腐蚀
C. 若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D. 若将该铜板与直流负极相连,则铁铜均难被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各微粒浓度关系正确的是( )
A.向氨水中滴加稀硫酸至溶液呈中性:c(NH4+)=c(SO![]() )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
B.向 l00mL 3 mol/L 的 NaOH 溶液中通入标准状况下体积为 4.48L 的 CO2:3c(Na+)=2[c(CO3 2-)+c(HCO3-)+c(H2CO3)]
C.CH3COONa 溶液中加入少量 KNO3 后溶液一定有:c(Na+)+c(H+)=(CH3COO 一)+c(OH 一)
D.等物质的量浓度的①NH4HSO4、②NH4HCO3、③NH4Cl 溶液中,c(NH4+)的大小关系:①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是
A. In是第五周期第ⅢA族元素
B. 11549In的中子数与电子数的差值为17
C. 原子半径:In>Al
D. 碱性:In(OH)3>RbOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。

已知:在溶液中.FeSO4+NO![]() [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法不正确的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法不正确的是
A. 装置F、I中的试剂依次为水、硫酸亚铁溶液
B. 若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
C. 实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D. 装置J收集的气体中一定不含NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:Zn(s) +![]() O2(g) =ZnO(s) ΔH1=-351.1kJ/mol
O2(g) =ZnO(s) ΔH1=-351.1kJ/mol
Hg(l) +![]() O2(g) = HgO(s) ΔH2=-90.7kJ/mol
O2(g) = HgO(s) ΔH2=-90.7kJ/mol
由此可知Zn(s) + HgO(s) = ZnO(s) + Hg(l)的ΔH3,其中ΔH3的值是
A.-260.4 kJ/molB.-254.6 kJ/molC.-438.9 kJ/molD.-441.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列溶液中微粒浓度关系一定正确的是( )
A.0.1mol·L-1Na2CO3溶液中,加水稀释,![]() 的值减小
的值减小
B.0.1mol·L-1的硫酸铝溶液中:c(SO42-)>c(Al3+)>c(H+)>c(OH-)
C.pH=7的氨水与氯化铵的混合溶液中:c(Cl-)>c(NH4+)
D.pH=2的醋酸溶液和pH=12的NaOH溶液等体积混合:c(Na+)=c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com