
【题目】[化学-选修5:有机化学基础]盐酸普鲁卡因是一种常见的局部麻醉剂,在传导麻醉、浸润麻醉及封闭疗法中均有良好的药效。其合成路线如下:
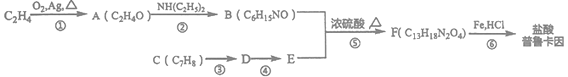
已知:①A的核磁共振氢谱为单峰,C为芳香烃。
②盐酸普鲁卡因的结构简式为:![]() 。
。
③![]() 。
。
④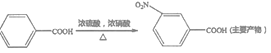 。
。
请回答下列问题:
(1)A的结构简式为_______________,C的化学名称为________________。
(2)反应①、③的反应类型分别为____________、________________。
(3)反应⑤的化学方程式为______________________。
(4)G是F的同系物,其相对分子质量比F小14。G的同分异构体能同时满足如下条件:
①1分子该物质可水解生成2分子CH3CH2OH。
②苯环上只有一种化学环境的H。
共有_______种(不考虑立体异构);请任意写出其中一种的结构简式_________________。
(5)写出用甲苯为原料制备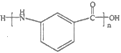 的合成路线________________(无机试剂任选)。
的合成路线________________(无机试剂任选)。
【答案】 ![]() 甲苯 氧化反应 取代反应
甲苯 氧化反应 取代反应 ![]() 7
7 
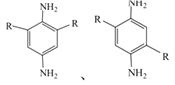 (-R为-COOCH2CH3)
(-R为-COOCH2CH3) 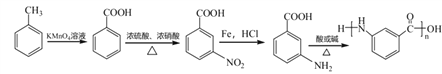
【解析】分析:本题为有机合成与推断题,所给合成路线并不复杂,但信息④有新意,注意应用,本题难度一般。
(1)根据核磁共振氢谱只有1个吸收峰,说明分子中只含有一种化学环境的氢原子,又因为是氧化反应,故可得A的结构式为![]() ;C的分子式C7H8属于芳香烃,名称为甲苯,因此,本题正确答案为:
;C的分子式C7H8属于芳香烃,名称为甲苯,因此,本题正确答案为:![]() ; 甲苯;
; 甲苯;
(2)根据合成线路图可知反应①为乙烯的催化氧化、反应③为甲苯的硝化反应,反应类型分别为氧化反应;取代反应,因此,本题正确答案为:氧化反应;取代反应;
(3)根据合成线路图可知反应⑤为酯化反应,B提供羟基,E提供羧基,化学方程式为:![]() ;
;
(4)F的结构简式为![]() ,G是F的同系物,其相对分子质量比F小14。G比F少一个CH2原子团,满足条件①1分子该物质可水解生成2分子CH3CH2OH。则说明含有两个-COOC2H5,苯环侧链没有多余的碳原子,也没有多余的氧原子,满足条件②苯环上只有一种化学环境的H,则该分子高度对称,符合条件的有:
,G是F的同系物,其相对分子质量比F小14。G比F少一个CH2原子团,满足条件①1分子该物质可水解生成2分子CH3CH2OH。则说明含有两个-COOC2H5,苯环侧链没有多余的碳原子,也没有多余的氧原子,满足条件②苯环上只有一种化学环境的H,则该分子高度对称,符合条件的有: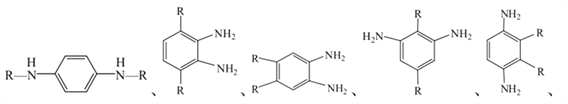
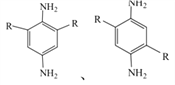 (-R为-COOCH2CH3) 共7种,所以,本题正确答案为: 7;
(-R为-COOCH2CH3) 共7种,所以,本题正确答案为: 7; 
 (-R为-COOCH2CH3)(其中任何一种)。
(-R为-COOCH2CH3)(其中任何一种)。
(5)采用逆合成法分析,要制备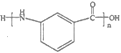 需要制得
需要制得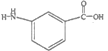 ,由于氨基和羧基处于间位,结合信息,甲苯先氧化后硝化,可在羧基的间位引入硝基,间硝基苯甲酸还原硝基,可得
,由于氨基和羧基处于间位,结合信息,甲苯先氧化后硝化,可在羧基的间位引入硝基,间硝基苯甲酸还原硝基,可得 ,该合成路线为:
,该合成路线为: 。
。


科目:高中化学 来源: 题型:
【题目】工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
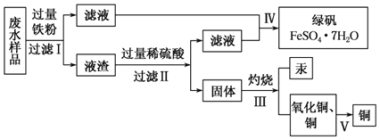
(1)步骤Ⅰ中加入过量铁粉的目的是_______________________________。
(2)步骤Ⅱ中________(填“能”或“不能”),用盐酸代替硫酸,写出步骤Ⅱ中涉及反应的化学方程式:____________________________________。
(3)步骤Ⅳ得到绿矾的操作蒸发浓缩______________、______________、洗涤、干燥。现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是___________。
(4)步骤 V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。从安全角度考虑,方案_________不好;从产品纯度考虑,方案_________不好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产以反水处理工业。工业上可由软锰矿(主要成分为MnO2)制备,目前有两种较为成熟的制法。其模拟流程如下图所示:
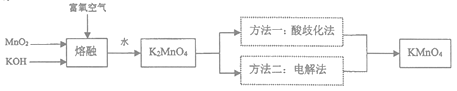
附表:不同温度下若干常见钾的化合物的溶解度(单位:g/(100gH2O))
化学式 | 20°C | 30°C | 40°C | 60°C | 80°C | 100°C |
CH3COOK | 256 | 283 | 324 | 350 | 381 | |
K2SO4 | 11.1 | 13 | 14.8 | 18.2 | 21.4 | 24.1 |
KCl | 34.2 | 37.2 | 40.1 | 45.8 | 51.3 | 56.3 |
KMnO4 | 6.34 | 9.03 | 12.6 | 22.1 | ||
K2CO3 | 111 | 114 | 117 | 127 | 140 | 156 |
(1)“熔融”时,可用作坩锅材质的是________________(填序号)。
A.氧化铝 B.陶瓷 C.氧化镁 D.石英
(2)写出MnO2和KOH熔融物中通入富氧空气时获得K2MnO4的化学方程式______________________。
(3)“酸歧化法”是在pH<6的情况下K2MnO4即可转化为MnO2和KMnO4,过滤除去MnO2,将滤液经过蒸发浓缩、趁热过滤得到KMnO4粗晶体,再经过重结晶获得较纯净的KMnO4晶体;
①根据表中的溶解度数据以及上述操作的特点,“酸歧化法”不适宜选择的酸性物质是________。
A.稀硫酸 B.醋酸 C.稀盐酸 D.二氧化碳
②“蒸发浓缩”时,温度需控制在70℃,适宜的加热方式是________________。
③根据相关方程式,计算“酸歧化法”的理论产率为_________________。
(4)“电解法”克服了“酸歧化法”理论产率偏低的问题,同时副产品KOH可用于软锰矿的焙烧。电解法制备高锰酸钾的实验装置示意图如下(图中阳离子交换膜只允许K+离子通过)
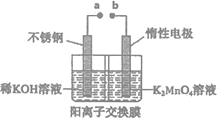
①a为______极(填“正”或“负”),右室发生的电极反应方程式为_______________。
②若电解开始时阳极区溶液为1.0L0.40mol·L-1K2MnO4溶液,电解一段时间后,右室中n(K)/m(Mn)为6:5,阴极区生成KOH的质量为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各氧化还原反应中,水既不作氧化剂,也不作还原剂的是( )。
A. 2F2+2H2O==4HF+O2 B. C+H2O![]() CO+H2
CO+H2
C. 2Na+2H2O==2NaOH+H2↑ D. Cl2+H2O==HCl+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,0.01 mol/L MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A. -69.4 kJ·mol-1 B. -45.2 kJ·mol-1
C. +69.4 kJ·mol-1 D. +45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的常见短周期元素,X的某种氢化物能使湿润的红色石蕊试纸变蓝.Y的一种核素质量数为18,中子数为10.在同周期元素中Z的简单离子半径最小,W的单质是良好的半导体材料。下列说法中正确的是
A. 简单气态氢化物稳定性:W >X
B. Y元素的相对原子质量为18
C. X2H4的分子中极性键和非极性键数目比为4:l
D. 电解Z的熔融氯化物可以冶炼单质Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是( )
A.分液时,分液漏斗下层液体从下口流出,上层液体从也从下口流出
B.蒸发结晶时应将溶液蒸至有大量固体析出时
C.蒸馏时,应使温度计水银球靠近蒸馏烧瓶底部
D.称量时,称量物放在称量纸上置于托盘天平右盘,砝码放在托盘天平左盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。则下列说法不正确的是
X | Y | |||
W | Z |
A.原子半径大小:Y<XB.W的简单气态氢化物比X的稳定
C.Z的最高价氧化物对应的水化物是一种强酸D.W的单质常用作半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com