
| | Na2CO3的质量 | 关于O2的描述 |
| A | 21.2g | O2的摩尔质量是36g·mol-1 |
| B | 21.6g | 生成标准状况下O2的体积为2.24L |
| C | 21.6g | O2的摩尔质量是34g·mol-1 |
| D | 22.4 g | 生成标准状况下O2的体积为2.24mL |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.在标准状况下,1mol水的体积是22.4L |
B.1mol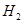 所占的体积一定是22.4L 所占的体积一定是22.4L |
C.1L0.5mol/L的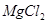 溶液中,含有 溶液中,含有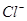 的个数为 的个数为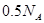 |
D.在标准状况下,总质量为28g的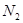 和CO的混合气体,其体积约为22.4L 和CO的混合气体,其体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 1 | 2 | 3 |
| m(混合物)/g | 4.6 | 7.2 | 7.9 |
| V(CO2)(标准状况)/L | 1.12 | 1.68 | 1.68 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg和Al | B.Al和Fe |
| C.Fe和Zn | D.Zn和Cu |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3mol NF3与水完全反应生成HNO3和NO,转移电子数2NA |
| B.4.4g14CO2含中子数2.4 NA |
| C.标准状况下,2.24L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.2NA |
| D.常温常压下,1.7g H2O2中含有的电子数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.3 mol/L | B.0.4 mol/L | C.0.5 mol/L | D.0.6 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol的2H35Cl含中子数为1.8NA |
| B.16g O3和O2混合物中氧原子数为NA |
| C.常温下,1L pH=l的溶液中H+的数目大于0.1NA |
| D.0.1 mol的H2O2中含有非极性键数为0.2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0 g | 75.0 g | 140.0 g |
| 反应后 | 37.0 g | 79.0 g | 140.5 g |

 Na2S + 4CO↑ ②Na2SO4 + 4CO
Na2S + 4CO↑ ②Na2SO4 + 4CO Na2S + 4CO2
Na2S + 4CO2 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com