
 如图是广州亚运会开幕式“红棉花开迎宾来”焰火盛宴的一个场景,请回答下列问题:
如图是广州亚运会开幕式“红棉花开迎宾来”焰火盛宴的一个场景,请回答下列问题:

科目:高中化学 来源: 题型:

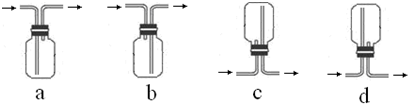
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4与C2H4 |
| B、C2H2与C3H6 |
| C、C2H4与C3H4 |
| D、CH4与C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铝制饮具最好不要盛放酸性或碱性较强的液体食物 | 因为Al和Al2O3既可以与酸反应,又可以与碱反应 | Ⅰ对,Ⅱ对,无 |
| B | 氯气不能使干燥的有色布条褪色,能使湿润的有色布褪色 | 说明次氯酸的氧化性比氯气强 | Ⅰ对,Ⅱ对,无 |
| C | 二氧化硫能使KMnO4溶液褪色 | 二氧化硫具有漂白性 | Ⅰ对,Ⅱ对,无 |
| D | 常温下,铁或铝制成的槽车可以密封贮运浓硫酸或浓硝酸 | 因为铁和铝与浓硫酸或浓硝酸发生钝化. | Ⅰ对,Ⅱ对,有 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、-(b-a) kJ?mol-1 |
| B、+(b-a) kJ?mol-1 |
| C、(b-a) kJ?mol-1 |
| D、(b+a) kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、①②③④ |
| C、①②③ | D、①②. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.0mol/L |
| B、1.5 mol/L |
| C、0.18 mol/L |
| D、0.24mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com