



科目:高中化学 来源:不详 题型:单选题
| A.它们都能在空气中燃烧生成M2O |
| B.它们失去电子的能力很强,故在自然界中无游离态存在 |
| C.它们的焰色反应都是黄色 |
| D.它们都能与水反应生成碱和氢气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶1 | B.2∶3 |
| C.4∶3 | D.3∶2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
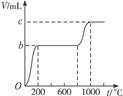
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①最少 | B.④最多 | C.③居中 | D.一样多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com