
| A. | nCH2=CHCH2COOH→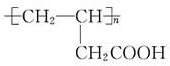 | |
| B. | nHOOC(CH2)5OH?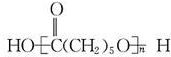 +(n-1)H2O +(n-1)H2O | |
| C. | n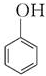 +nHCHO$\stackrel{H+}{→}$ +nHCHO$\stackrel{H+}{→}$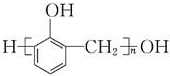 +(2n-1)H2O +(2n-1)H2O | |
| D. | nHOOC(CH2)4COOH+nHO(CH2)2OH?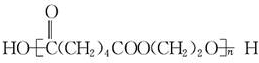 +(2n-1)H2O +(2n-1)H2O |
分析 A.CH2=CHCH2COOH中含碳碳双键,可发生加聚反应;
B.HOOC(CH2)5OH中含-OH、-COOH,可发生缩聚反应;
C. 与HCHO发生酚醛缩合反应;
与HCHO发生酚醛缩合反应;
D.HOOC(CH2)4COOH与HO(CH2)2OH发生缩聚反应.
解答 解:A.CH2=CHCH2COOH中含碳碳双键,可发生加聚反应,反应为nCH2=CHCH2COOH→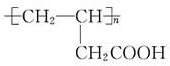 ,故A正确;
,故A正确;
B.HOOC(CH2)5OH中含-OH、-COOH,可发生缩聚反应,反应为nHOOC(CH2)5OH?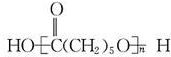 ,故B错误;
,故B错误;
C. 与HCHO发生酚醛缩合反应,反应为n
与HCHO发生酚醛缩合反应,反应为n +nHCHO$\stackrel{H+}{→}$
+nHCHO$\stackrel{H+}{→}$ +(2n-1)H2O,故C正确;
+(2n-1)H2O,故C正确;
D.HOOC(CH2)4COOH与HO(CH2)2OH发生缩聚反应,反应为nHOOC(CH2)4COOH+nHO(CH2)2OH?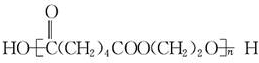 +(2n-1)H2O,故D正确;
+(2n-1)H2O,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机合成反应为解答的关键,侧重分析与应用能力的考查,注意缩聚反应的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
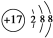 ②羟基的电子式:
②羟基的电子式: ;③HClO的结构式:H-Cl-O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质; ⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化( )
;③HClO的结构式:H-Cl-O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质; ⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化( )| A. | ①②⑤ | B. | ①④⑥⑦ | C. | ②③④⑥ | D. | ②③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
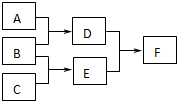 单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系:(有部分反应物或者生成物未标出)
单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系:(有部分反应物或者生成物未标出)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胃酸过多的病人,可以服用碳酸氢钠来中和胃酸 | |
| B. | 晶体硅是在通信工程中制作光导纤维的主要原料 | |
| C. | 溴化银见光易分解,是一种重要的感光材料,是胶卷中必不可少的成分 | |
| D. | 由于镁燃烧发出耀眼的白光,因此常用来制造信号弹和焰火 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | |
| B. | 标准状况下,11.2 L H2O中含有的氢原子数为NA | |
| C. | H2O2分解产生1molO2,转移的电子数为4NA | |
| D. | 1 mol•L-1 CuCl2溶液中含有的氯离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②、③或④ | B. | ②、③或⑤ | C. | ①、③或⑤ | D. | ①、③或④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com