
| 烯烃被氧化的部位 | CH2═ | RCH═ |  |
| 氧化产物 | CO2 | RCOOH |  |
 ),则该烯烃结构简式可能是( )
),则该烯烃结构简式可能是( )| A. |  | B. |  | ||
| C. | CH2=CH-CH=CHCH2CH3 | D. |  |
分析 某烯烃与酸性KMnO4溶液作用后得到的氧化产物有CO2、乙二酸(HOOC-COOH)和丙酮(  ),则分子中应含有CH2═、=CH-CH=以及=C(CH3)2等结构,以此解答该题.
),则分子中应含有CH2═、=CH-CH=以及=C(CH3)2等结构,以此解答该题.
解答 解:A.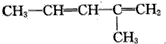 与酸性KMnO4溶液作用后得到的氧化产物有乙酸,二氧化碳,和HCOOCOCH3,故A错误;
与酸性KMnO4溶液作用后得到的氧化产物有乙酸,二氧化碳,和HCOOCOCH3,故A错误;
B.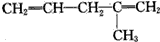 与酸性KMnO4溶液作用后得到的氧化产物有二氧化碳和HCOOCH2COCH3故B错误;
与酸性KMnO4溶液作用后得到的氧化产物有二氧化碳和HCOOCH2COCH3故B错误;
C. CH2=CH-CH=CHCH2CH3与酸性KMnO4溶液作用后得到的氧化产物有乙二酸,二氧化碳,和丙酸,故C错误;
D.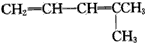 与酸性KMnO4溶液作用后得到的氧化产物有乙二酸,二氧化碳和丙酮,故D正确.
与酸性KMnO4溶液作用后得到的氧化产物有乙二酸,二氧化碳和丙酮,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握题给信息,把握有机物的结构和性质的关系,难度不大.


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | AgNO3(AgNO3) | B. | NaOH(NaOH) | C. | NaCl(NaCl) | D. | CuCl2(CuCl2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 2 mol•L-1盐酸 | B. | 500 mL2mol•L-1硫酸 | ||
| C. | 50 mL 3 mol•L-1盐酸 | D. | 50 mL 18.4 mol•L-1硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将废弃的电池、金属、纸制品等垃圾分类回收 | |
| B. | 用铝制容器盛放浓硫酸,是因为常温下铝遇浓硫酸发生钝化 | |
| C. | 新型材料聚碳酸酯纤维,石墨烯纤维都属于有机高分子 | |
| D. | 地沟油经过加工处理制肥皂或生物柴油,实现厨余废物利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成化合物种类最多的原子 | |
| B. | M层有5个电子的原子 | |
| C. | N层上电子数与K层电子数相等,次外层有8个电子的原子 | |
| D. | 原子核外最外层电子数等于电子层数的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石转化成石墨是自发进行的过程 | |
| B. | 石墨转化成金刚石是自发进行的过程 | |
| C. | 金刚石比石墨更稳定 | |
| D. | 金刚石比石墨能量低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷微溶于水,其密度小于空气的密度 | |
| B. | 甲烷使溴的四氯化碳溶液褪色,发生取代反应 | |
| C. | 甲烷在氧气中燃烧,发生氧化反应 | |
| D. | 甲烷能使酸性高锰酸钾溶液褪色,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{22}^{48}Ti$和${\;}_{22}^{50}Ti$原子中均含有22个中子 | |
| B. | ${\;}_{22}^{48}Ti$和${\;}_{22}^{50}Ti$在元素周期表中占有相同的位置 | |
| C. | ${\;}_{22}^{48}Ti$和${\;}_{22}^{50}Ti$的物理性质相同 | |
| D. | ${\;}_{22}^{48}Ti$和${\;}_{22}^{50}Ti$为同一核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇与甲醚(CH3OCH3)都可作燃料电池的燃料.
甲醇与甲醚(CH3OCH3)都可作燃料电池的燃料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com