
 �����ǹ�ҵ��������Ҫ�IJ�Ʒ֮һ���ںܶ���������Ҫ��;���ش��������⣺
�����ǹ�ҵ��������Ҫ�IJ�Ʒ֮һ���ںܶ���������Ҫ��;���ش��������⣺| ѹǿ SO2ת���� �¶� | ��1.0��105Pa | ��5.0��105Pa�� | ����1.0��106Pa | ��1.5��106Pa�� |
| ��400�� | ��0.9961 | ��0.9972 | ��0.9984 | ��0.9989 |
| ��500�� | ��0.9675 | ��0.9767 | ��0.9852 | ��0.9894 |
| ��600�� | ��0.8528 | ��0.8897 | ��0.9276 | ��0.9468 |
���� ���������û�����ȼ�չ�ҵ�Ʊ�����Ĺ�ҵ�����⣬�漰����¯����ķ�Ӧ����ΪSO2�Ĵ������ǿ��淴Ӧ���Ƿ��ȷ�Ӧ����Ӧ���ڽӴ�������У������Ƚ���������Ӧ��Ԥ�ȣ�����������������Ļ�����壬��SO3�ܽ���ˮ���ȣ���Ũ��������SO3���������Ч�ʣ�β����ѡ���ð�ˮ���գ���ֹ��Ⱦ���������Ϊ�����ݴ˷������⣮
��1�����ݻ��������Ҫ�ɷ�ΪFeS2������ʱ��O2��Ӧ����Fe2O3��SO2�����������յ��豸�Ƿ���¯��
��2��SO2ת��ΪSO3�ڽӴ����н��У�����SO2��O2�ķ�ӦΪ���淴Ӧ������C�������������У�SO2��SO3��O2��Ϊ�˷�ֹ�������γɣ���98.3%��H2SO4����SO3������SO3���豸����������
��3������SO2��ת���ʼ������ɱ���ѡ��
��4����߷�Ӧ���ʺ�SO2��ת���ʣ�����Ӱ�컯ѧ��Ӧ���ʺͻ�ѧƽ���ƶ������жϣ�
��5������SO2Ϊ�����������Ӧ�����κ�ˮ��д��
��� �⣺��1�����������Ҫ�ɷ�ΪFeS2������ʱ��O2��Ӧ����Fe2O3��SO2����ѧ����ʽΪ��4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3+8SO2�����������յ��豸�Ƿ���¯���ʴ�Ϊ��4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3+8SO2������¯��
��2��SO2ת��ΪSO3�ڽӴ����н��У�SO2��O2�ķ�ӦΪ���淴Ӧ������C�������������У�SO2��SO3��O2��Ϊ�˷�ֹ�������γɣ���98.3%��H2SO4����SO3������SO3���豸�����������ʴ�Ϊ���Ӵ��ң� SO3��SO2��O2����������98.3%��H2SO4��
��3����ΪSO2��O2�ķ�Ӧ�Ƿ��ȷ�Ӧ������ѡ����¶�Ϊ400�棬��1��������ѹʱSO2��ת�����Ѿ��ܴ�������ѹǿ��SO2��ת������߲��������������ɱ�������ѡ��1��������ѹ���ʴ�Ϊ��400�棬1��������ѹ��
��4��A�����º���ͨ����ƽ���ص����壬��ѹ����ѹ���䣬ƽ�ⲻ������������ת���ʲ��䣻��A����
B������������������Ӧ��Ũ������Ӧ��������ʹƽ��������У�����˶��������ת���ʣ���B��ȷ��
C������ֻ�ı����ʲ��ı�ƽ�⣬���ı�ת���ʣ���C����
D�������¶ȣ���ʱת��SO3 ����ʹƽ��������У���������ת�����������·�Ӧ���ʼ�С����D����
��ѡB��
��5��SO2Ϊ�����������Ӧ�����κ�ˮ����ѧ����ʽΪ��2NH3•H2O+SO2=��NH4��2SO3+H2O���ʴ�Ϊ��2NH3•H2O+SO2=��NH4��2SO3+H2O��
���� ���⿼���˹�ҵ����������ɹ��̺ͷ�Ӧ��������������Ĵ�������Ӧ������ѡ��β�����յķ����жϣ���������Ӵ��Ҵ�������Ӧ��ƽ���ƶ�����Ŀ�Ѷ��е�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150ml 1mol/L�Ȼ�����Һ | B�� | 150ml 3mol/L�Ȼ�����Һ | ||
| C�� | 75ml 2mol/L�Ȼ����Һ | D�� | 50ml 1mol/L�Ȼ�ͭ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ����SO42- | B�� | һ����CO32- | ||
| C�� | ����ȷ��Cl-�Ƿ���� | D�� | ����ȷ��SO42- �Ƿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Na2CO3��Һ��BaSO4����ת��ΪBaCO3���� | |
| B�� | �����¶ȣ���ѧƽ�ⷢ���ƶ�����Ϊƽ�ⳣ���ı� | |
| C�� | �������ȣ�ˮ��MgCO3��ת��Ϊ�����ܵ�Mg��OH��2 | |
| D�� | �ı�һ��Ӱ������ʹ��ѧƽ�ⷢ���ƶ�����ƽ�ⳣ��Kֵһ���仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
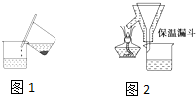
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˹����ʵ�����������غ㶨�ɵ����� | |
| B�� | ��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ/mol����0.5mol H2SO4��Ũ�����뺬1 mol NaOH����Һ��ϣ��ų�����������57.3 kJ | |
| C�� | ��C��ʯī����C�����ʯ����H=+73 kJ/mol����֪ʯī�Ƚ��ʯ�ȶ� | |
| D�� | ��101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com