
| A. | 过滤、蒸馏、萃取 | B. | 过滤、结晶、升华 | C. | 分液、溶解、萃取 | D. | 溶解、过滤、结晶 |
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 腐蚀中正极反应为:2H++2e-=H2↑ | |
| B. | 腐蚀中负极反应为:Fe-3e-=Fe3+ | |
| C. | 钢铁设备上连接铜块可以防止腐蚀 | |
| D. | 钢铁与外加直流电源的正极相连可以防止腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br- | B. | OH- | C. | HCO3- | D. | NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4CO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | B. | 2Na2O2+2 H2O═4NaOH+O2↑ | ||
| C. | H2O+Cl2?HCl+HClO | D. | NH3+SO2+H2O═NH4HSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及其离子方程式 | 评价 |
| A | 少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | 正确 |
| B | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓ | 错误.溴乙烷不能电离出Br- |
| C | Ca(HCO3)2溶液与等物质的量NaOH溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O | 错误.Ca2+与HCO3-的物质的量之比为1:2 |
| D | 氢氧化钡溶液与等物质的量的稀硫酸混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
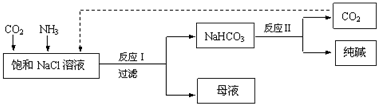
| A. | 反应Ⅰ原理为CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl | |
| B. | 向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3 | |
| C. | 反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱 | |
| D. | 往母液中通入氨气,加入细小的食盐颗粒并降温,可使氯化铵析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com