
科目:高中化学 来源: 题型:
(08安徽六校联考)(18分)某同学设计下列装置进行铁和浓H2SO4反应的实验探究,请回答下列问题。
(1)将16克铁粉放入烧瓶中,由分液漏斗放入18mol/L的浓H2SO420mL,结果没有任何反应现象,原因是__随后点燃A处酒精灯,就有气体产生了(2分)
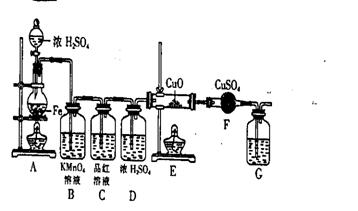 (2)随着反应的进行,B中酸性KMnO4溶液颜色逐渐变浅,请用离子方程式表示_______(3分)C中品红溶液颜色始终没有变化。
(2)随着反应的进行,B中酸性KMnO4溶液颜色逐渐变浅,请用离子方程式表示_______(3分)C中品红溶液颜色始终没有变化。
(3)当G处有持续稳定的气泡时,再点燃E处酒精灯,这样操作的原因是______3分)
(4)反应进行一段时间后,E、F处可观察到明显的现象,其中E中的反应方程式是___(3分),F处可看到的实验现象是___(3分)
(5)为了确保实验的严谨性和F中现象的可信性,G中盛放的液体可以是___________(4分)
A. CaCl2溶液 B. Ca(OH)2溶液 C. 浓硫酸 D. CCl4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com