
原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是______(填元素符号,下同),第一电离能最小的是________;
 (2)C所在的主族元素气态氢化物中,沸点最低的是______(填化学式);
(2)C所在的主族元素气态氢化物中,沸点最低的是______(填化学式);
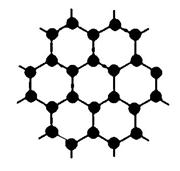
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为____________;
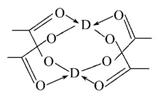 (4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是______(填选项序号);
(4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是______(填选项序号);
①极性键 ②非极性键
③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:
D单质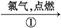 棕色的烟
棕色的烟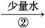 绿色溶液
绿色溶液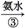 蓝色沉淀
蓝色沉淀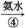 蓝色溶液
蓝色溶液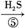 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:__________。
科目:高中化学 来源: 题型:
在一固定容积的密闭容器中进行着如下反应:
CO2(g) + H2(g)  CO(g) + H2O(g)
CO(g) + H2O(g)
其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1) K的表达式为: ;
(2) 该反应的正反应为 反应(“吸热”或“放热”)
(3) 能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
E.容器中气体密度不变 F.1mol H—H键断裂的同时断裂2 mol H-O键
(4) 在850℃时,可逆反应:CO2(g) + H2(g)  CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2 O ( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
3min—4min达到平衡时CO的平衡浓度c3= (c3精确到小数点后面三位数),CO2 (g)的转化率= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列反应中,改变反应物的用量或浓度,不会改变生成物的是( )
A.铜和硝酸反应
B.二氧化碳通入氢氧化钠溶液中
C.细铁丝在氯气中燃烧
D.氯化铝与氢氧化钠溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
请在标有序号的空白处填空。
(1)可正确表示原子轨道的是____①____。
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)原子的电子排布式:____②____。
(3)下列物质变化,只与范德华力有关的是__③____。
A.干冰熔化
B.乙酸汽化
C.乙醇与丙酮混溶
D.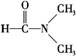 溶于水
溶于水
E.碘溶于四氯化碳
F.石英熔融
(4)下列物质中,只含有极性键的分子是____④____,既含离子键又含共价键的化合物是____⑤____;只存在σ键的分子是____⑥____,同时存在σ键和π键的分子是____⑦____。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6
F.CaCl2 G.NH4Cl
(5)用“>”“ <”或“=”填空:
第一电离能的大小:Mg____⑧____Al;
熔点的高低:KCl____⑨____MgO。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于某些离子的检验及结论一定正确的是( )
A.加入硝酸银溶液产生白色沉淀,则一定有Cl-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO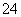
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH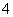
D.通入氯气,然后加入硫氰化钾溶液,溶液变为红色,一定含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的下列溶液中,符合按pH由小到大的顺序排列的是( )
A.Na2CO3 NaHCO3 NaCl NH4Cl
B.Na2CO3 NaHCO3 NH4Cl NaCl
C.(NH4)2SO4 NH4Cl NaNO3 Na2S
D.NH4Cl (NH4)2SO4 Na2S NaNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
甲苯是由苯环和甲基结合而成的,甲苯能够使酸性KMnO4溶液褪色是因为( )
A.烷烃能使酸性KMnO4溶液褪色
B.苯环能使KMnO4酸性溶液褪色
C.苯环使甲基的活性增强而导致的
D.甲基使苯环的活性增强而导致的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.锥形瓶可用作加热的反应器
B.室温下,不能将浓硫酸盛放在铁桶中
C.配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高
D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com