
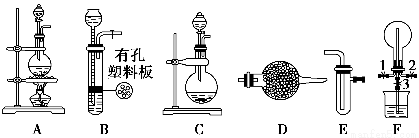
某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空:
Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与________(填装置编号)连接;装置C中的烧瓶内固体宜选用________。
a.碱石灰 b.氯化钙c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是________________。
(3)装置F可用于探究氯气与氨气(已知氯气与氨气可发生反应:3Cl2+2NH3===N2+6HCl)的反应。实验时打开弹簧夹1、3,关闭2,先向烧瓶中通入________,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子______________________________________________________________________________。
Ⅱ.探究某些物质的性质
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,能证明结论的实验现象是______________________________________________________。
(5)若利用装置A、E进行乙烯与溴水反应的实验,写出反应的化学方程式________________________________________________________________。
(6)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。F的烧瓶中发生反应的化学方程式为______________________;F的烧杯所起的作用是________________________________________________________________。
(1)D ad (2)饱和食盐水、浓硫酸
(3)氯气 取少量固体于试管中,加入适量浓NaOH溶液并加热,在管口用湿润的红色石蕊试纸检验产生的气体,若湿润的红色石蕊试纸变蓝,[或用蘸有浓盐酸(或浓硝酸)的玻璃棒放在试管口,若有白烟生成],证明固体中有NH4+
(4)装置E中的NaBr溶液变橙红色
(5)CH2==CH2+Br2―→Br—CH2—CH2—Br
(6)SO2+2H2S===3S↓+2H2O 吸收尾气
【解析】 (1)制取NH3,可用浓氨水的分解制备,然后再用碱石灰或生石灰干燥,但不能用CaCl2,因为CaCl2可结合NH3生成CaCl2·8NH3。(2)制取干燥纯净的Cl2,可用饱和食盐水除HCl,再用浓H2SO4干燥Cl2。(3)应向烧瓶中先通Cl2,再通NH3,因为Cl2有颜色,便于观察;一开始若通NH3,由于弹簧夹3打开,容易形成喷泉。证明NH4+要注意“操作→现象→结论”,同时还要注意细节,如浓NaOH,加热,湿润等。(4)可利用Cl2+2NaBr===2NaCl+Br2,证明还原性Br->Cl-。(5)CH2==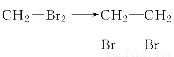 。(6)SO2+2H2S===3S↓+2H2O;F可用来吸收剩余的SO2或H2S。
。(6)SO2+2H2S===3S↓+2H2O;F可用来吸收剩余的SO2或H2S。


科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题2常用化学计量--物质的量练习卷(解析版) 题型:选择题
设阿伏加德罗常数的数值为NA,则下列说法中正确的是( )。
A.1.0 L 0.1 mol·L-1 Na2S溶液中含有的S2-离子数小于0.1NA
B.1 mol氯气与过量的Fe反应,转移电子的数目为3NA
C.2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA
D.50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题12化学实验基础练习卷(解析版) 题型:选择题
下列装置或操作错误的是(双选)( )。

A.甲图所示装置可以检验有乙烯生成
B.乙图所示装置可以制取金属锰
C.丙图所示装置用来洗气,除去CO2中的HCl气体
D.丁图所示装置用来分离乙醇和乙酸
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题11有机化学基础练习卷(解析版) 题型:填空题
茉莉花香气的成分有多种,乙酸苯甲酯是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:

(1)写出反应①的化学方程式:______________________________________。
(2)反应③的反应类型为______________。
(3)写出C中的官能团的名称:_______________________________________。
(4)上述①②③三个反应中,原子的理论利用率为100%,符合绿色化学要求的反应是________(填序号)。
(5)乙酸苯甲酯有很多同分异构体,含有酯基和一取代苯结构的同分异构体有五种,其中三种的结构简式是

请写出另外两种同分异构体的结构简式:_____________和_____________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题11有机化学基础练习卷(解析版) 题型:选择题
下列说法正确的是( )。
A.乙炔和苯均为不饱和烃,都只能发生加成反应
B.加新制的Cu(OH)2悬浊液并加热可检验尿液中的葡萄糖
C.油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂
D.向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题10常见非金属元素及其重要化合物练习卷(解析版) 题型:选择题
从下列实验事实中得到的结论,正确的是(双选) ( )。
选项实验事实结论
A将纯铜片和另一种金属M用导线连接,同时插入稀硫酸中,铜片表面有气泡冒出 金属活动性:M>Cu
B将SO2通入酸性KMnO4溶液中,红色褪去SO2有漂白性
CCO2通入苯酚钠溶液中,出现浑浊酸性:苯酚<碳酸
DCl2的水溶液可以导电Cl2是电解质
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 综合实验设计练习卷(解析版) 题型:实验题
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学设计了如下实验方案探究反应原理并验证产物。
(1)提出假设
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为________;
猜测2:白色不溶物可能为MgCO3;
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证猜测:
实验序号 | 实验 | 实验现象 | 结论 |
实验Ⅱ | 将实验 Ⅰ 中收 集到的气体点燃 | 能安静燃烧、产 生淡蓝色火焰 | 气体成分为 __①__ |
实验Ⅲ | 取实验 Ⅰ 中的白 色不溶物,洗涤, 加入足量__②__ | __③__ | 白色不溶物可能含有MgCO3 |
实验Ⅳ | 取实验 Ⅰ 中的澄 清液,向其中加入 少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在__④__ |
(3)为进一步确定实验Ⅰ的产物,设计定量实验方案,如图所示:

称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8 g,装置B增重8.8 g,试确定白色不溶物的化学式为_____________________________________________。
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡的原因:______________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 基本概念、基本理论练习卷(解析版) 题型:填空题
脱硫技术能有效控制SO2对空气的污染。
(1)向煤中加入石灰石可减少燃烧产物中SO2的含量,该反应的化学方程式是
_______________________________。
(2)海水呈弱碱性,主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42—、Br-、HCO3—等。含SO2的烟气可利用海水脱硫,其工艺流程如图所示:

①向曝气池中通入空气的目的是_____________________________________。
②通入空气后曝气池中海水与天然海水相比,浓度有明显不同的离子是________。
a.Cl- b.SO42— c.Br- d.HCO3—
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可得到NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。

①图中a极要连接电源的________(填“正”或“负”)极,C口流出的物质是________。
②SO32—放电的电极反应式为____________________________。
③电解过程中阴极区碱性明显增强,用平衡移动的原理解释原因:
__________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮专题复习物质的组成分类及能量变化练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有C 的个数为0.1NA
的个数为0.1NA
B.标准状况下22.4 L H2O所含分子数为NA
C.1 L 0.5 mol·L-1 CH3COOH溶液中,CH3COO-的个数为0.5NA
D.在NO、NO2的混合气体22.4 L中,含有的氮原子数为NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com