
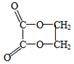
以乙醇为原料,用下述6类反应:①氧化②消去③加成④酯化⑤水解⑥加聚,来合成环乙二酸乙二酯(结构如右图),正确的顺序是( )
A. ①⑤②③④ B. ①②③④⑤ C. ②③⑤①④ D. ②③⑤①⑥
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
水是一种宝贵的自然资源。
(1)生活污水中,常含N、P化合物而造成水体植物富营养化污染。水中的氨在微生物的作用下,可发生以下一系列变化:A、 NH3 + O2 →HNO2+ H2O(未配平)
B、2HNO2+O2 → 2HNO3,回答以下问题
① 配平反应A并标出电子转移的方向与数目:
____NH3+ ___O2 → ___HNO2+ ____ H2O
② 反应B中被氧化的元素是 。
(2)氧化还原法是处理污水常用的方法之一。某工厂排放的污水,经检测,污水中含有
0.012 mol/L的游离态溴,可用Na2SO3还原除去污水中的溴,请写出其离子方程式:
若处理5L这种污水,至少需加入0.05mol/L的Na2SO3溶液 L才能将单质溴全部除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中属于取代反应的是( )
①由乙醇制备乙烯 ②乙酸和乙醇反应制备乙酸乙酯 ③丙烯和溴的四氯化碳溶液反应
④苯和浓硝酸、浓硫酸共热 ⑤乙酸乙酯和稀硫酸共热 ⑥溴乙烷和氢氧化钠的水溶液共热
A.①②④⑤ B.②④⑤⑥ C.②③④⑤ D.①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、W、R、T是前17号元素中的5种,X、Y位于同主族,Y原子的最外层电子数与次外层电子数相等,R原子的最外层电子数为次外层电子数的3倍,T无正价,W单质用于制造计算机芯片,下列说法不正确的是( )
A.气态氢化物稳定性:W<T B.离子半径:X<R
C.最高价氧化物对应水化物碱性:X>Y D.Y单质能与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法正确的是
A.混合气体中一定有甲烷 B.混合气体中一定是甲烷和乙烯
C.混合气体中一定有乙烷 D.混合气体中一定有乙炔(CH≡CH)
查看答案和解析>>
科目:高中化学 来源: 题型:
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol·L-1氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是( )。
A.c= B.p=m+
B.p=m+
C.n=m+17Vc D. m<p<
m<p<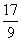 m
m
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图所示。
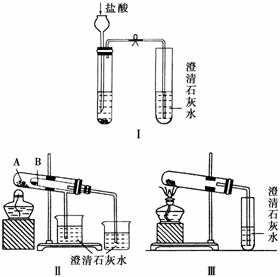
(1)只根据图Ⅰ所示实验,不能够达到实验目的的原因是
________________________________________________________________________。
(2)图Ⅱ、Ⅲ所示实验均能鉴别这两种物质,其反应的化学方程式为____________;
与实验Ⅲ相比,实验Ⅱ的优点是(填选项代号)________。
A.Ⅱ比Ⅲ复杂
B.Ⅱ比Ⅲ安全
C.Ⅱ比Ⅲ操作简便
D.Ⅱ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅱ验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是(填化学式)________。
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当石灰水过量时,其离子方程式为_________________________________________。
②当碳酸氢钠与氢氧化钙物质的量之比为2∶1时,所得溶液中溶质的化学式为________,请设计实验检验所得溶液中溶质的阴离子__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式___________________________________________________________。
(2)根据等电子原理,写出CO分子的结构式_________________________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是________________________________;
甲醛分子中碳原子轨道的杂化类型为___________________。
②甲醛分子的空间构型是__________________;1 mol甲醛分子中σ键的数目为____________。
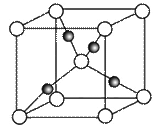
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu+数目为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com