
 已知25℃时,几种难溶电解质的溶度积如下表所示:
已知25℃时,几种难溶电解质的溶度积如下表所示:| 化学式 | AgCl | Ag2S | AgOH |
| 溶度积(K甲 ) | 1.8×10-10 | 6.3×10-50 | 1.5×10-8 |
A、
| ||
B、
| ||
C、
| ||
D、
|
| 1 |
| 2 |
| [S2-] |
| [Cl-] |
| ||
| [AgNO3]?[V2-V1] |
| V1 |
| 2(V2-V1) |


科目:高中化学 来源: 题型:
| A、水解反应、加成反应、氧化反应 |
| B、加成反应、水解反应、氧化反应 |
| C、水解反应、氧化反应、加成反应 |
| D、加成反应、氧化反应、水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此时醋酸和氢氧化钠溶液恰好中和 | ||
| B、溶液中存在未电离的醋酸分子 | ||
C、用含a的代数式表示醋酸(HAc)的电离常数为Ka=
| ||
| D、a肯定大于0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
| B、硅酸盐NaAISiO4.nH2O可改写成氧化物形式为:Na2O.AI2O3.2SiO2.2nH2O |
| C、AI65Cu23Fe12是一种拟晶,具有合金的优良物理性能,其硬度比金属Al、Cu、Fe都大 |
| D、过量铁与浓硫酸加热反应可以得到氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入NaOH溶液后,溶液颜色变浅 |
| B、对2HI(g)?H2(g)+I2(g)平衡体系,增大压强可使颜色变深 |
| C、反应CO+NO2?CO2+NO△H<0,升高温度可使平衡向逆反应方向移动 |
| D、工业合成氨工艺中,采用较高的压强来提高原料的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
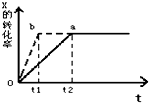 图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)?2Z(g)+W(g);△H=QkJ/mol 的反应过程. 若使a曲线变为b曲线,可采取的措施是( )
图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)?2Z(g)+W(g);△H=QkJ/mol 的反应过程. 若使a曲线变为b曲线,可采取的措施是( )| A、增大Y的浓度 |
| B、加入催化剂 |
| C、降低温度 |
| D、增大体系压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO3的水解:SO3 2-+2H2O?H2SO3+2OH- |
| B、NaHCO3的电离:NaHCO3?Na++H++CO3 2- |
| C、KHS的电离:KHS=K++HS- |
| D、NaClO溶液与FeCl2溶液混合:2ClO-+Fe2++2H2O=2HClO+Fe(OH)2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com