
【题目】反应A+B→C(反应放热)分两步进行:①A+B→X(反应吸热),②X→C(反应放热)。下列示意图中,能正确表示总反应过程中能量变化的( )
A. 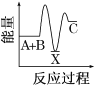 B.
B. 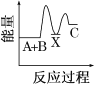
C. 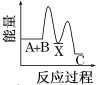 D.
D. 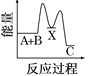
科目:高中化学 来源: 题型:
【题目】在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图中所示的实验方法、装置或操作正确的是( )
|
|
A.测量锌与稀硫酸反应的速率 | B.证明非金属性:Cl>C>Si |
|
|
C.进行酸碱中和滴定实验 | D.测定中和热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 16g CH4含有的原子数为NA
B. 17 g OH- 含有的质子数为9NA
C. 2g D2气体中含有的中子数为0.5 NA
D. 标准状况下22.4 L NH3含有的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于油和脂肪的比较,错误的说法是 ( )。
A.油的熔点低,脂肪的熔点高
B.油含不饱和烃基的相对量比脂肪少
C.油和脂肪都不易溶于水,易溶于汽油、酒精、苯等有机溶剂
D.油经过氢化可以转化为脂肪,通常又叫做硬化油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的短周期部分,表中字母分别表示一种元素。

请回答下列问题:
(1)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)____。
a.MnO2 b.NaCl c.Na2SO3 d.KMnO4
(2)d、e、h四种元素最高价氧化物对应的水化物的酸性由弱到强的顺序为(用化学式表示)________。b、c、f、g、h形成的简单离子的半径由小到大的顺序为_______(用离子符号填写)。
(3)在1L的密闭容器中,通入1molf2气体和3mola2气体,一定温度下反应生成fa3气体,2min时,测得f2的浓度为0.75mol·L-1,则2min时fa3的物质的量为_____mol;反应达到平衡状态时,若增大fa3的产率,可以采取措施(填序号)_____。
①升高温度 ②恒容充入氦气
③向密闭容器内充入f2气 ④及时分离出fa3气体
(4)d与a可形成化合物d5a12,试写出它的一氯取代物有一种的同分异构体的结构简式_____。
(5)a、d两种元素可形成多种化合物,其中化合物X的产量是衡量一个国家石油化工发展水平的标志。X可与H2O在一定条件下反应生成化合物乙醇,该反应的化学方程式为:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年,M IT的唐纳德·撒多维教授领导的小组研制出一种镁锑液态金属储能电池。电池突破了传统电池设计理念,以NaCl、KCl和MgCl2的熔融盐作为电解质。以Mg和Sb两极金属,整个电池在700℃工作,处在液体状态。由于密度的不同,在重力下分层,分别形成上层金属Mg,下层金属Sb和中间的NaCl、KCl及MgCl2电解质层。电池的工作原理如图所示,关于该电池的说法不正确的是 ( )
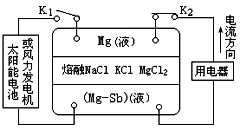
A. 电池充电时Cl—从上向下移动
B. 电池放电时正极的电极反应式为Mg2++2e—=Mg
C. 电池充电时阳极的电极反应式为:2Cl—-2e—=Cl2↑
D. 电池充电时中层熔融盐的组成不发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某元素的原子结构示意图: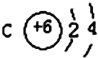 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
(2)已知某元素的原子结构示意图: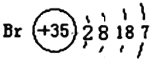 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】x、y、z、w、n为五种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
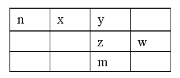
请回答下列问题:
(1)w位于周期表中第__________周期,第__________族。
(2)n、z、w、三种元素最高价氧化物水化物的酸性由弱到强的顺序为:__________(用化学式表示)。
(3)下列事实能说明y元素的非金属性比z元素的非金属性强的是____
A.y单质与z的气态氢化物水溶液反应,溶液变浑浊
B.在氧化还原反应中,1moly单质比1molz得电子多
C.y和z两元素的简单氢化物受热分解,前者的分解温度高
D.y元素最高价氧化物水化物酸性比z元素最高价氧化物水化物酸性强
(4)y和氢元素形成的10电子微粒中常见![]() 价阳离子为__________(填化学式);z和氢元素形成的18电子微粒中常见
价阳离子为__________(填化学式);z和氢元素形成的18电子微粒中常见![]() 价阴离子的电子式为__________。
价阴离子的电子式为__________。
(5)化合物nyz存在于天然气中,可以用NaOH溶液洗涤除去。化合物nyz的电子式为__________,其与NaOH溶液反应除生成两种正盐外,还有水生成,其化学方程式为__________。
(6)m元素的原子序数为__________,它是一种__________。(填“金属”或“非金属”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com