
国外新近研制的溴化锌蓄电池的基本构造是用碳棒作两极,溴化锌溶液作电解液. 现有四个电极反应:①Zn﹣2e=Zn2+ ②Zn2++2e=Zn ③Br2+2e=2Br﹣ ④2Br﹣﹣2e=Br2.那么,充电时的阳极和放电时的负极反应分别是()
A. ④① B. ②③ C. ③① D. ②④
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
NO2通过盛有水的洗气瓶,转移0.02mol电子时,参加反应的NO2气体在标准状况下的体积为()
A. 224mL B. 336mL C. 448mL D. 672mL
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 单位物质的量的气体所占的体积就是气体摩尔体积
B. 摩尔是物质的量的单位
C. 阿伏加德罗常数就是6.02×1023
D. CO2的摩尔质量为44g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量
B. 热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据
C. 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态
D. 凡是化合反应都是放热反应,分解反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图装置探究铁在海水中的电化学腐蚀与防护.下列说法不正确的是()
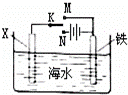
A. 若X为锌棒,开关K置于M处,可减缓铁的腐蚀,采用了牺牲阳极的阴极保护法
B. 若X为锌棒,开关K置于N处,X极的反应:4OH﹣﹣4e﹣=O2↑+2H2O
C. 若X为碳棒,开关K置于N处,可减缓铁的腐蚀,采用了外加电流的阴极保护法
D. 若X为碳棒,开关K置于M处,X极的反应:O2+4e﹣+2H2O=4OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,
(1))请写出NO2和CO反应的热 化学方程式: 已知:N2 (g)+2NO2 (g)⇌4NO(g)△H=+292.3kJ•mol﹣1,
化学方程式: 已知:N2 (g)+2NO2 (g)⇌4NO(g)△H=+292.3kJ•mol﹣1,
则反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g) 的△H= ;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生反应:4NO2(g)+O2(g)⇌2N2O5(g);已知体系中n(NO2)随时间变化如表:
t(s) 0 500 1000 1500
N(NO2)(mol) 20 13.96 10.08 10.08
写出该反应的平衡常数表达式:K= ,
已知:K3000C>K3500C,则该反应是 反应(填“放热”或“吸热”).

查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 3.6g重水中含有的中子数为2NA
B. 16.0g的过氧(根)离子中含有的电子数为9NA
C. 100mL 3.0mol/L的盐酸与5.6g铁屑完全反应转移的电子数为0.3NA
D. 含2mol H2SO4的浓硫酸与足量金属铜完全反应,产生SO2分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子既能与镁粉反应,又能大量共存,且其溶液为无色溶液的是( )
A. Ca2+、Cl﹣、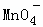 、Na+ B. K+、Cl﹣、
、Na+ B. K+、Cl﹣、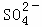 、H+
、H+
C. OH﹣、Na+、Al3+、I﹣ D. H+、Cl﹣、Ba2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生下列反应aA(g)⇌cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是()
A. 平衡向正反应方向移动 B. a<c+d
C. D的体积分数变大 D. A的转化率变大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com