
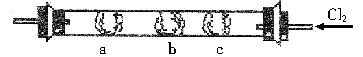
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 16(c-a) |
| b-c |
| 16(c-a) |
| b-c |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
.一硬质玻璃管的两端装有带导管的塞子,左、中、右分别放有3个湿棉球(如图所示)。c球浸有淀粉碘化钾溶液;b球浸有碘化钾浓溶液;a球浸有溴化钾溶液。实验时,从右端缓缓通入氯气,同时在b处微热,并逐渐向左移动酒精灯。则可观察到:在a处有____色的____产生;在b处有____色的____产生;c球变成____色;稍冷却后,b、c之间的管壁上有____色的____析出。通过实验可以判定Cl2、Br2、I2的氧化性____最强,Cl-、Br-、I-的还原性_____最弱。
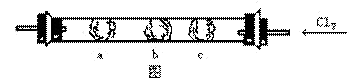
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com