
A.0.1 mol.L-1 B.1.5 mol.L-1 C.0.25 mol.L-1 D.0.5mol.L-1
| 在MgCl2、KCl、Na2SO4的混合溶液中,存在着金属离子与酸根离子的如下关系:
Mg2+ ~ 2Cl-,K+ ~ Cl-,2Na+ ~ SO42-。据题意和上述离子物质的量浓度的关系,由c(SO42-)可求c(Na+),由c(Cl-)、c(K+)+c(Na+)的关系可求出c(Mg2+)为0.5mol.L-1,但这种方法容易在导出过程中出错。较为简便的方法是:利用混合溶液中各种阴、阳离子的正负电荷的总数为零,溶液呈电中性列等式:(设溶液为V L)。 V×c(Mg2+)×2+V×c(K+)×1+V×c(Na+)×1=V×c(Cl-)×1+V×c(SO42-)×2 2 c(Mg2+)+(c(K+)+c(Na+))=c(Cl-)+2 c(SO42-), ∴c(Mg2+)=(1.5+0.5×2-1.5)×2=0.5 mol.L-1。
|


科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:022
在含MgCl2、KCl和Na2SO4三种物质的混合溶液中,已知:c(Cl-)=1.5 mol.L-1,c(SO42-)=0.5 mol.L-1, c(K+)+c(Na+)=1.5 mol.L-1,则c(Mg2+)应是( )
A.0.1 mol.L-1 B.1.5 mol.L-1 C.0.25 mol.L-1 D.0.5mol.L-1
查看答案和解析>>
科目:高中化学 来源:09~10年建湖二中高二下学期期末考试化学卷 题型:实验题
(10分)江苏省拥有很长的海岸线,具有丰富的海洋资源,因此盐化工是本省的一个重要产业。从盐卤初步得到的光卤石(KCl·MgCl2·6H2O)晶体中,还含有约8%的NaCl。
为了从光卤石中提取KCl和MgCl2,某学习小组查阅资料得到MgCl2、KCl和NaCl在不同温度下的溶解度S(g/100g水)的数据如下:
并设计出下面的实验流程:
根据他们提供的数据和实验回答下列问题:
问题1:以上实验流程中晶体X的化学式为 ,若制得的X还含有少量的可溶性杂质,可用
的方法进一步提纯。操作步骤①中趁热过滤的原因是:
问题2:工业上采用电解无水氯化镁的方法制取金属镁。
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:
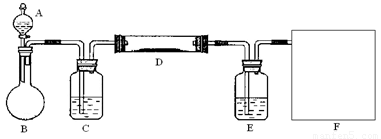
(2)该小组同学采取将浓硫酸滴入浓盐酸制取氯化氢气体的方法,用下图的实验装置,在干燥的HCl气流中加热MgCl2·6H2O来得到无水MgCl2。装置中盛有浓硫酸的仪器分别
是 (填写仪器的符号),需要加热的仪器是 (同上)。
(3)为防止对环境的污染,还需要将尾气吸收,但实验室现有的仪器和试剂只有:烧杯、导管、蒸馏水、酒精、苯、四氯化碳。请你为他们设计一个尾气的吸收装置,将装置图画在方框内并在图中标明所用试剂。
查看答案和解析>>
科目:高中化学 来源:09-10年建湖二中高二下学期期末考试化学卷 题型:实验题
(10分)江苏省拥有很长的海岸线,具有丰富的海洋资源,因此盐化工是本省的一个重要产业。从盐卤初步得到的光卤石(KCl·MgCl2·6H2O)晶体中,还含有约8%的NaCl。
为了从光卤石中提取KCl和MgCl2,某学习小组查阅资料得到MgCl2、KCl和NaCl在不同温度下的溶解度S(g/100g水)的数据如下:
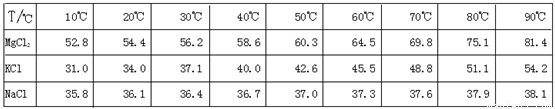
并设计出下面的实验流程:

根据他们提供的数据和实验回答下列问题:
问题1:以上实验流程中晶体X的化学式为 ,若制得的X还含有少量的可溶性杂质,可用
的方法进一步提纯。操作步骤①中趁热过滤的原因是:
问题2:工业上采用电解无水氯化镁的方法制取金属镁。
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:
(2)该小组同学采取将浓硫酸滴入浓盐酸制取氯化氢气体的方法,用下图的实验装置,在干燥的HCl气流中加热MgCl2·6H2O来得到无水MgCl2。装置中盛有浓硫酸的仪器分别
是 (填写仪器的符号),需要加热的仪器是 (同上)。
(3)为防止对环境的污染,还需要将尾气吸收,但实验室现有的仪器和试剂只有:烧杯、导管、蒸馏水、酒精、苯、四氯化碳。请你为他们设计一个尾气的吸收装置,将装置图画在方框内并在图中标明所用试剂。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com