
ͭ�������仯�����ڹ�ҵ��ũҵ���Ƽ����ճ��������й㷺Ӧ�á�
��1����ҵ�����û�ͭ����Ҫ�ɷ���Cu2S��ұ��ͭ��Ϊ�˲ⶨ��ͭ����Ʒ�Ĵ��ȣ������Ը��������Һ��Ӧ(��֪1 molCu2Sʧȥ10mol�ĵ���)��д���÷�Ӧ�����ӷ���ʽ ��
��2����ҵ�����÷�ͭм�����ᣨ�����ᡢ���ᣩΪ��Ҫԭ���Ʊ�����ͭ���塣ij����c(HNO3)=2 mol��L��1��c(H2SO4)=4 mol��L��1�ķ�����Һ100 mL�����������������������������Ʊ�����ͭ���壨CuSO4��5H2O��������Ϊ ��
��3������һ�麬��ͭ�̵�ͭƬ�����費���������ʣ��ڿ�������������ȫ��Ӧ�����ⶨ����Ӧǰ������������ͬ������֪������������= ��
��
������ͭƬ��ͭ��������Ϊ ���������2λ��Ч���֣�
�ڹ�̬ͭ������������Ӧ�������仯����ͼ��ʾ��д����̬ͭ��������Ӧ����1 mol��̬������ͭ���Ȼ�ѧ����ʽ ��
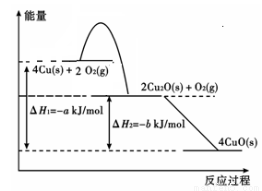
��4��������������Դ�����������й㷺��;����������(K2FeO4) ����ǿ�����ԣ���ɱ������������Fe(OH)3�������ԣ���һ�����;�ˮ����������ͼ��ʾ��װ�ÿ�����ȡ�����ĸ�����ء�
����֪���������صķ�ӦʽΪ��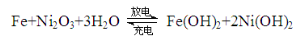 ��
��
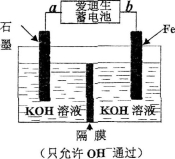
�ٰ��������صĸ���������
��д����ȡ������������ĵ缫��Ӧʽ
�۵�����19.8g��K2FeO4ʱ����Ĥ������Һ�������仯��(��m��һ��m��)Ϊ_ g��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ�����и�һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ԭ�ӽṹģ�͵��ݱ�ͼ���ң����з�����ʷ�ݱ�˳���һ��������
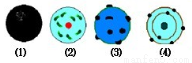
A���ŢǢƢ� B���ŢƢǢ�
C���ŢȢǢ� D���ŢǢȢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
19����ĩ�����ʼ�ҿ�ԭ���ڲ��ṹ�����ܣ����ȷ��ֵ��ӵĿ�ѧ����
A��������ѧ�������� B��Ӣ������ѧ����ķ��
C�����������ѧ�Ұ����ӵ��� D��Ӣ����ѧ�ҵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У���˵��SiO2���������������
��SiO2��4HF===SiF4����2H2O ��SiO2��CaO CaSiO3
CaSiO3
��SiO2��2NaOH===Na2SiO3��H2O ��SiO2��2C Si��2CO��
Si��2CO��
A���٢� B���ڢ� C���ۢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ��һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У�ˮ�Ȳ�����������Ҳ���ǻ�ԭ��������Ӧ��������ԭ��Ӧ����
A��2Na2O2��2H2O��4NaOH��O2�� B��C��H2O CO��H2
CO��H2
C��Na2O��H2O��2NaOH D��2F2��2H2O��4HF��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������и���11���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����л���ͬ���칹����Ŀ�жϴ������
ѡ�� | �л��� | ͬ���칹����Ŀ |
A | ����ʽΪC5H12 | 3 |
B | ����ʽΪC5H10����ʹ������Ȼ�̼��Һ��ɫ | 5 |
C | ����ʽΪC4H10O������Na��Ӧ�������� | 4 |
D | ����ʽΪC4H8O2����NaHCO3��Ӧ | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��������У���˸���12���¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
���÷�����X��ϩ��Y���Ժϳ����������ռ�BAD��
��֪��G���ܷ���������Ӧ��B��FeCl3��Һ����ɫ��C��D�Ĺ���Ϊ�����Ȼ�����COOH���ķ�Ӧ������BAD�ṹ��ʽΪ��
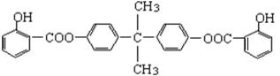
BAD�ĺϳ�·�����£�
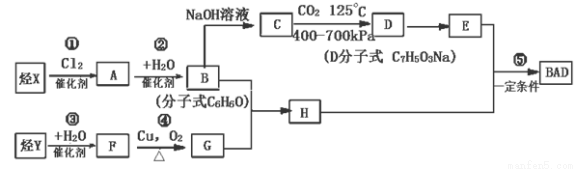
�Իش��������⣺
��1��д���ṹ��ʽ��Y ��D ��
��2����������ȡ����Ӧ���� ����������ţ���
��3��1molBAD�����뺬 molNaOH����Һ��ȫ��Ӧ��
��4��д�����з�Ӧ�Ļ�ѧ����ʽ��ע����Ӧ��������Ӧ��
B+E
��5��E�ж���ͬ���칹�壬�жϷ�������Ҫ���ͬ���칹����ĿΪ �֡�
���ܷ���������Ӧ ����FeCl3��Һ����ɫ �ۺ˴Ź�������ͼ�����ĸ����շ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ����12�������������Ͽ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
�̵Ļ������������Ĵ����������ڸɵ��ԭ�������ȡ�
��1��п�̸ɵ�صķ�ӦΪ2MnO2 +Zn+2NH4Cl =2 MnO(OH) +Zn(NH3)2Cl2��MnO(OH)����Ԫ�صĻ��ϼ�Ϊ____��
��2����ϵ�ػ�ԭ��ķ�Һ������Mn2+��Fe2+��Zn2+�ȣ�����εμ�Na2S��Һ���������ɵij���Ϊ ���ѧʽ����[��֪Ksp(MnS)=1.4��10-1 5��Ksp(ZnS)=2.9��10 -25��Ksp(FeS)=6��0��10-18]
��3�� Mn2+��H2O2�֡�������
2H2O2(l)=2H2O(l)+O2(g) ��H1���䷴Ӧ�������£�
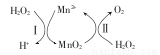
����֪��Ӧ��ΪMnO2(s)+H2O2��1�� +2H+( aq)=Mn2+(aq) +O2(g)+2H2O��1�� ��H2��д����ӦI���Ȼ�ѧ����ʽ���ʱ��á�H1�͡�H2��ʾ���� ��
��ij�¶�ʱ����10 mL0.4 mol��L-1 H2O2Һ�е���1��MnSO4�����֡�������
2H2O2 =2H2O+O2����ò�ͬʱ������O2�����(������Ϊ��״���µ����)���±���
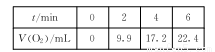
0��2 minʱ��Ӧ���ʱ�2��4 minʱ�Ŀ죬��ԭ����_________��
0��6 min��ƽ����Ӧ����v(H2O2)= ��������Һ����ı仯����
��4���̻������Ǻϳɼ״��������ѵĴ�������֪��

�ٷ�ӦI������Ӧ�� ������ȡ������ȡ�����Ӧ��
�ڷ�Ӧ���ƽ�ⳣ������ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��һ��ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����ȷ����
A��H2SO4��Ba(OH)2��Һ��Ӧ��Ba2++OH��+H++SO42��=BaSO4��+H2O
B��CH3COOH��Һ��NaOH��Һ��Ӧ��H++ OH��=H2O
C������ϡ���ᷴӦ��Fe+2H+=Fe2++H2��
D��������Cu(OH)2��Ӧ��H++ OH-��=H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com