
常温,相应条件下,下列各组离子一定能大量共存的是
| A.c(Al3+)=0.1mol/L的溶液中:Na+、K+、AlO2-、OH- |
| B.无色溶液中:K+、CH3COO-、HCO3-、MnO4- |
C.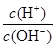 =1×1014的溶液:Ba2+、Na+、SO32-、NO3- =1×1014的溶液:Ba2+、Na+、SO32-、NO3- |
| D.通入足量CO2后所含离子还能大量共存的是:K+、Ca2+、NO3-、Cl- |
科目:高中化学 来源: 题型:单选题
下列表示对应化学反应的离子方程式正确的是
| A.漂白粉露置在空气中:ClO-+CO2+H2O=HClO+HCO3- |
| B.用过量氨水吸收二氧化硫:SO2+NH3·H2O=HSO3-+NH4+ |
| C.用足量的氢氧化钠溶液吸收二氧化氮:3NO2+2OH-=2NO3-+NO+H2O |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在室温下,下列各组微粒在溶液中能大量共存的是
| A.Na+、Ba2+、OH-、Cl- | B.H+、Fe2+、ClO-、SO42- |
| C.K+、Fe3+、C6H5O-、SCN- | D.NH4+、Al3+、SiO32-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在无色水溶液中能大量共存的一组离子是
| A.Na+、Ag+、Br-、MnO4- | B.K+、Al3+、AlO2-、SO42- |
| C.Fe3+、H+、I-、SO32- | D.Mg2+、NH4+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法正确的是( )
| A.一个SiO2分子中含有2个Si—O键,一个C2H4中含5对共用电子 |
| B.给铁皮镀锌可以有效的防止铁的电化学腐蚀 |
| C.金属氧化物和硝酸反应都只生成盐和水 |
| D.在强电解质水溶液中电解质全都以自由移动的离子形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在某无色透明的酸性溶液中,能大量共存的离子组是
| A.Na+ 、K+、SO42-、HCO3- | B.Na十、Ba2+、NO3-、SO42- |
| C.Na+、 K+、Cl-、 NO3- | D.Fe3+、K+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是
| A.Na2CO3和HCl | B.NaHCO3和Ba(OH)2 | C.NaAlO2和H2SO4 | D.AgNO3和NH3·H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(8分)往100 mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的CO2的体积V(标准状况)与M的质量W的关系如下图所示。试解答下列问题:
(1)A点时,白色固体M的化学式为____________________,通入的CO2的体积为________ mL (标准状况下,下同)。
(2)C点时,白色固体M的化学式为____________________,通入的CO2的体积为________ mL。
(3)B点时M的组成成分为________(用化学式表示),通入的CO2的体积为________ mL。
(4)该NaOH溶液的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如下:
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。PbO2的氧化性大于MnO2。PbSO4是一种微溶物质。有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
| 离子 | 离子半径(pm) | 开始沉淀 时的pH | 完全沉淀 时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com