
反应 2A=B+3C,在20℃时进行,v(A)=5mol/(L•s),已知每升温10℃,该反应速率增大到原来的2倍,则当其它条件不变而温度升到50℃时,反应速率v(B)是()
A. 20 mol/(L•s) B. 40 mol/(L•s) C. 60 mol/(L•s) D. 15 mol/(L•s)
考点: 反应速率的定量表示方法.
专题: 化学反应速率专题.
分析: 温度每升高10℃反应速率是原来的2倍,以此计算反应速率.
解答: 解:10℃时以某物质表示的反应速率为5mol/L•s,由温度每升高10℃反应速率是原来的2倍可知,在20℃时进行,v(A)=5mol/(L•s),
30℃、40℃、50℃的反应速率分别为10mol/L•s、20mol/L•s、40mol/L•s;速率之比等于化学方程式计量数之比,v(B)=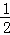 v(A)=
v(A)=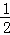 ×40mol/L•s=20mol/L•s;
×40mol/L•s=20mol/L•s;
故选A.
点评: 本题考查温度与反应速率的关系,注意把握信息“每升高10℃反应速率是原来的2倍”是解答的关键,题目难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
下列每组中各有三对物质,它们都能用分液漏斗分离的是()
A. 乙酸乙酯和水,酒精和水,植物油和水
B. 四氯化碳和水,溴苯和水,硝基苯和水
C. 甘油和水,乙酸和水,乙酸和乙醇
D. 汽油和水,苯和水,己烷和水
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的离子方程式有 ;
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应中,收集产生的气体,记录获得相同体积的气体所需时间.
实验 A B C D E F
混
合
溶
液 4mol/LH2SO4/mL 30 V1 V2 V3 V4 V5
饱和CuSO4/mL 0 0.5 2.5 5 V6 20
H2O/mL V7 V8 V9 V10 10 0
时间(min) 15 10 5 3 6 9
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因 ;
(3)改用锌粉与稀硫酸反应,加入少量硫酸铜溶液后充分振荡,一段时间剩余少量固体.该同学对固体成分提出下列假设:
假设1:全部为铜;
假设2: .
(4)请你设计实验验证上述假设1,完成下表内容.
实验方案(不要求写具体操作过程) 预期实验结果和结论
,
查看答案和解析>>
科目:高中化学 来源: 题型:
家用炒菜锅用水清洗后,出现红棕色的锈斑.在此变化过程中不发生的化学反应是()
A. 4Fe(OH)2+2H2O+O2═4Fe(OH)3
B. 2Fe+2H2O+O2═2Fe(OH)2
C. 正极反应:2H2O+O2+4 e﹣→4OH﹣
D. 负极反应:Fe→Fe3++3 e﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应N2+3H2⇌2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示.下列关系中能说明反应已达到平衡状态的是()
A. 3v正(N2)=v正(H2) B. v正(N2)=v正(NH3)
C. v正(H2)=3v逆(NH3) D. 3v正(N2)=v逆(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
含Ba(OH)2l mol的稀溶液与足量稀盐酸反应,放出114.6kJ的热量,表示该反应中和热的热化学方程式正确的是()
A. Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l);△H=﹣114.6kJ/mol
B. Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l);△H=+114.6kJ/mol
C.  Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)= BaCl2(aq)+H2O(l);△H=﹣57.3kJ/mol
BaCl2(aq)+H2O(l);△H=﹣57.3kJ/mol
D.  Ba(OH)2(aq)+HCl(aq)=
Ba(OH)2(aq)+HCl(aq)= BaCl2(aq)+H2O(l);△H=+57.3kJ/mol
BaCl2(aq)+H2O(l);△H=+57.3kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,等质量的O2和CO2相比较,下列叙述错误的是()
A. 密度比为8:11 B. 分子个数之比为11:12
C. 物质的量之比为11:8 D. 原子个数之比为11:12
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质:①KI ②铜 ③稀硝酸 ④NH3 ⑤NaHSO4  ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水
(1)按物质的分类方法填写表格的空白处(填物质编号)
分类标准 电解质 盐 非电解质 混合物
属于该类的物质
(2)上述某两种物质在溶液中可发生离子反应:H++OH﹣═H2O,写出该离子反应对应的化学方程式 .
(3)物质①的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com