
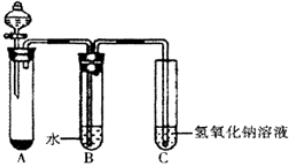
���� ��1���˷�Ӧװ��ΪŨ����Ͷ������̹����Ʊ��������Դ�д�����ӷ���ʽ��
��2��������ˮ��Ӧ����HCl��HClO�����������������Ӷ�������ˮ�����ԣ�ʪ�����ɫʯ����ֽ������ɫ��HClO����Ư���ԣ�
��3�������ж���ֱ���ŷ�����Ⱦ�����������ܹ����������Ʒ�Ӧ���������������գ�
��4���ٽ��������ԭ��Ӧ�л��ϼ�������ȣ��ж�ClO2��ClԪ�ػ��ϼ۱仯��Ԫ�ػ��ϼ����߱��ֻ�ԭ�ԣ�Ԫ�ػ��ϼ۽��ͱ��������ԣ�
�ڽ�Cl2ͨ������й���NaClO2�ķ�Ӧ���ڶ��߷�Ӧ���Ƶ�ClO2��NaClO2��Cl��+3�����ߵ�+4�ۣ�Cl2��ClԪ�صĻ��ϼ۴�0�۽��͵�-1�ۣ��䷴ӦΪ2NaClO2+Cl2�T2ClO2+2NaCl����Ϸ�Ӧ��֮��Ĺ�ϵ���㣬1molCl2���Ի��2mol���ӣ�1molClO2���Ի�õ���5mol���ӣ���
��� �⣺��1����Ӧװ��AΪŨ����Ͷ������̹����Ʊ�������װ�ã������ӷ���ʽΪ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
��2��������ˮ��Ӧ����HCl��HClO�����������������Ӷ�������ˮ�����ԣ�ʪ�����ɫʯ����ֽ������ɫ������������ˮ������ɫʯ����ֽ���ȱ��ɫ��HClO����Ư���ԣ���ʹ��ɫʯ����ֽƯ�ף����Կ����������ǣ���ɫʯ����ֽ�ȱ��ɫ����ɫ��������˵����ˮ�������Ժ�Ư���ԣ�
�ʴ�Ϊ���ۣۢ�
��3�������ж���Ҫ������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��4���ٷ�Ӧ��FeԪ�ء�MnԪ�ػ��ϼ����ߣ����ݻ��ϼ�������ȣ�ClO2��ClԪ�ػ��ϼ۽��ͣ����������ԣ�
�ʴ�Ϊ��������
�ڽ�Cl2ͨ������й���NaClO2�ķ�Ӧ���ڶ��߷�Ӧ���Ƶ�ClO2��NaClO2��Cl��+3�����ߵ�+4�ۣ�Cl2��ClԪ�صĻ��ϼ۴�0�۽��͵�-1�ۣ��䷴ӦΪ2NaClO2+Cl2�T2ClO2+2NaCl�������ı�״����11.2L Cl2����0.5mol������ClO2Ϊ1mol��������Ϊ1mol��67.5g/mol=67.5g��1molCl2���Ի��2mol���ӣ�1molClO2���Ի�õ���5mol���ӣ�
�ʴ�Ϊ��67.5��ClO2��
���� ���⿼��������ʵ�鷽����ơ�������ԭ��Ӧ�ļ��㣬���ؿ������������������ԭ��Ӧ�е�ʧ������ȣ��������ʵ����ʽ��������ԭ��Ӧ�����������Ŀ�Ѷ��еȣ�


 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+ | B�� | NH4+ | C�� | Ne | D�� | F- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
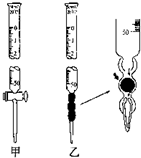 ijѧϰС����0.80mol/L��Ũ�ȵ��ռ���Һ�ⶨδ֪Ũ�ȵ����ᣮ
ijѧϰС����0.80mol/L��Ũ�ȵ��ռ���Һ�ⶨδ֪Ũ�ȵ����ᣮ| ʵ���� | ����HCl��Һ�����/mL | ����NaOH��Һ�����/mL |
| 1 | 20.00 | 22.00 |
| 2 | 20.00 | 22.10 |
| 3 | 20.00 | 21.90 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
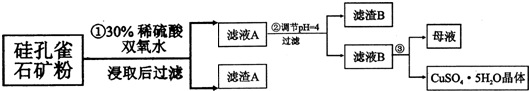
| �������� | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| ��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 |
| ������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ƿ���ܽ��������ƹ��岢������Һ | |
| B�� | ��100mL����Ͳ��ȡ5.2mL������ | |
| C�� | ��������ƽ��ȡ25.2gNaCl | |
| D�� | �÷�Һ©��������NaCl��Һ����ɳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
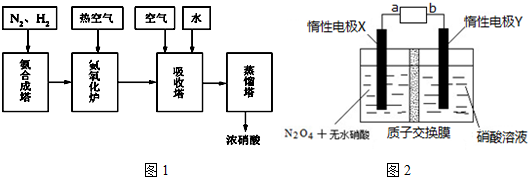
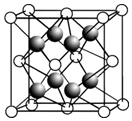 ��1������VSEPRģ���жϣ�������������ԭ�Ӷ���ͬһƽ���ϵ�һ����B��
��1������VSEPRģ���жϣ�������������ԭ�Ӷ���ͬһƽ���ϵ�һ����B��| ������/kJ•mol-1 | I1 | I2 |
| ͭ | 746 | 1958 |
| п | 906 | 1733 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com