
【题目】25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为( )
A.75%B.50%C.25%D.12.5%
【答案】C
【解析】
乙烷的分子式为C2H6,1mol乙烷完全燃烧生成液态水的方程式为:![]() ,因此1mol乙烷完全燃烧生成液态水会使气体总物质的量减少2.5mol;乙炔的分子式为C2H2,1mol乙炔完全燃烧生成液态水的方程式为:
,因此1mol乙烷完全燃烧生成液态水会使气体总物质的量减少2.5mol;乙炔的分子式为C2H2,1mol乙炔完全燃烧生成液态水的方程式为:![]() ,因此1mol乙炔完全燃烧生成液态水会使气体总物质的量减少1.5mol;丙烯的分子式为C3H6,1mol丙烯完全燃烧生成液态水的方程式为:
,因此1mol乙炔完全燃烧生成液态水会使气体总物质的量减少1.5mol;丙烯的分子式为C3H6,1mol丙烯完全燃烧生成液态水的方程式为:![]() ,因此1mol丙烯完全燃烧生成液态水会使气体总物质的量减少2.5mol,与乙烷的相同;不妨假设32mL中乙炔的体积为xmL,那么乙烷和丙烷的总体积为(32-x)mL;根据上述的燃烧规律列式:
,因此1mol丙烯完全燃烧生成液态水会使气体总物质的量减少2.5mol,与乙烷的相同;不妨假设32mL中乙炔的体积为xmL,那么乙烷和丙烷的总体积为(32-x)mL;根据上述的燃烧规律列式:![]() ,解得x=8mL,所以乙炔的体积分数为25%,C项正确;
,解得x=8mL,所以乙炔的体积分数为25%,C项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】已知反应X(g)+Y(g)=Z(g)+W(g)的能量变化如图所示,下列有关该反应的说法中错误的是
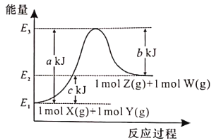
A.断开1molX(g)和1molY(g)中的化学键,要吸收akJ能量
B.1molZ(g)和1molW(g)所具有的能量为bkJ
C.每生成1molZ(g)和1molW(g)吸收ckJ能量
D.升高温度,可加快该反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收废水中苯酚的过程如图所示。下列分析错误的是

A. 操作I中苯作萃取剂
B. 苯酚钠在苯中的溶解度比在水中的大
C. 通过操作II苯可循环使用
D. 三步操作均需要分液漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
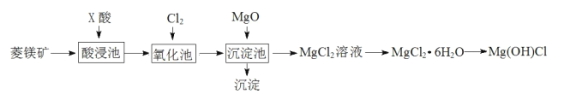
【题目】某同学利用菱镁矿(主要含MgCO3,FeCO3杂质)制取碱式氯化镁[Mg(OH)Cl]的流程。已知:MgO用于调节沉淀池中溶液的pH值。
金属离子 | pH | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Mg2+ | 8.8 | 11.4 |
下列说法不正确的是( )
A.酸浸池中加入的![]() 酸可以是硫酸
酸可以是硫酸
B.加入MgO后的沉淀一定含有Fe(OH)3
C.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
D.制得碱式氯化镁的方程式为:MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑
Mg(OH)Cl+HCl↑+5H2O↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家艾哈迈德·泽维尔使“运用激光技术观察化学反应时分子中原子的运动”成为可能,在他的研究中证实了光可诱发下列变化:这一事实可用于解释人眼的夜视功能,有关X、Y的叙述不正确的是( )
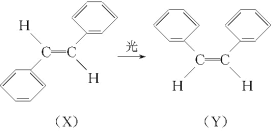
A.X和Y互为同分异构体
B.X和Y发生聚合反应生成的高分子化合物为纯净物
C.X和Y都可发生加聚反应
D.X和Y分子中所有原子可以处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用下列实验装置制备并研究SO2的性质,请按要求回答下列问题(夹持装置和A中加热装置已省略)。

操作步骤择要如下:
Ⅰ.打开活塞K,先通入一段时间N2,再关闭活塞K,加热A一段时间;
Ⅱ.A中不再产生气体后,停止加热,打开活塞K,缓慢通入氮气直至A装置冷却。
(1)装有Cu粒的仪器名称是________。
(2)实验室可用亚硫酸钠与浓硫酸制取SO2,该化学方程式是_______。
(3)下列说法正确的是____
A. 装置应在加入药品后检验装置气密性
B. 操作Ⅱ中继续通入氮气可以避免溶液出现倒吸
C. 装置A中的浓硫酸体现出了强氧化性、酸性
D. 装置B和装置D中都出现了褪色,是因为SO2有漂白性
(4)装置C中出现白色浑浊,请用离子方程式解释原因:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
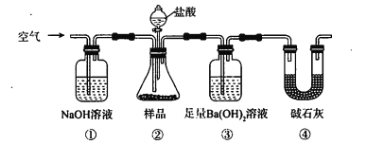
下列说法不正确的是
A. 必须在②③间添加吸收HCl的装置
B. ④的作用是防止空气中的气体影响实验的精确度
C. 通入空气的作用是保证②中产生的气体完全转移到③中
D. 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+O2(g)===CO2(g) ΔH1
CO2(g)+C(s)===2CO(g) ΔH2
2CO(g)+O2(g)===2CO2(g) ΔH3
4Fe(s)+3O2(g)===2Fe2O3(s) ΔH4
3CO(g)+Fe2O3(s)===3CO2(g)+2Fe(s) ΔH5
下列关于上述反应焓变的判断正确的是
A. ΔH1>0,ΔH3<0B. ΔH2>0,ΔH4>0C. ΔH1=ΔH2+ΔH3D. ΔH3=ΔH4+ΔH5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和硅均为元素周期表中第IV A族的元素,其单质和化合物有着重要应用。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式________。石墨烯中C的杂化类型为________。
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为________mol。

③石墨烯加氢制得的石墨烷,可用![]() 表示。下列有关叙述正确的是________。
表示。下列有关叙述正确的是________。
a.石墨烷属于烷烃 b.石墨烷难溶于水
c.石墨烷中所有碳原子共平面 d.石墨烷可以发生加成反应
④石墨烯可由加热![]() 晶体脱除
晶体脱除![]() 的方法制得。该过程属于________。
的方法制得。该过程属于________。
a.物理变化 b.分解反应 c.氧化还原反应
(2)![]() 的晶体结构与晶体硅类似。
的晶体结构与晶体硅类似。![]() 的晶体类型为________,晶体中
的晶体类型为________,晶体中![]() 原子与
原子与![]() 键的数目之比为________。
键的数目之比为________。
(3)![]() 与
与![]() 空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:__________________________。
空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com