
| 1.5mol |
| 3L |
| △n(B2) |
| △n(X) |
| 3 |
| a |
| 3.6mol |
| 3L×2min |
| 1 |
| 3 |
| 1 |
| 3 |
| 1.5mol |
| 3L |


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
| 煅烧 |
| H2O |
| NaOH(aq) |
| 电解 |
| 稀H2SO4 |
| 在空气中灼烧 |
| 蒸发 |
| 提取NaCl |
| Na2CO3溶液 |
| NaBr |
| NaBr |
| Cl2 |
| 热空气 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水玻璃与硅胶均属于酸 |
| B、漂白液与漂粉精的主要成分均为钠盐 |
| C、NO2、SO3均属于酸性氧化物 |
| D、醋酸、一水合氨均属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
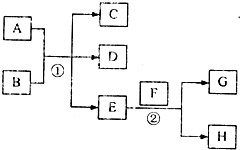 已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)
已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主食 | 米饭 |
| 副食 | 土豆、白菜、萝卜汤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度计插入液体测量温度,同时用它搅拌液体 | ||
B、给试管内液体加热时,液体体积不应超过试管容积的
| ||
| C、浓硫酸与酒精混合,将酒精加入到浓硫酸中 | ||
| D、为加速固体物质的溶解,常采用振荡、搅拌、加热等措施 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com