

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 2OH-+H2��+Cl2��
2OH-+H2��+Cl2�� 2OH-+H2��+Cl2��
2OH-+H2��+Cl2�� 2MgCl2��s��+Ti����Ar�����н��е������ǣ�
2MgCl2��s��+Ti����Ar�����н��е������ǣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
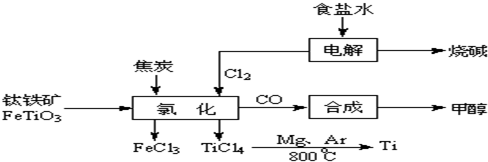
��(Ti )����Ϊ��������֮��ĵ�������������ͼ��ʾ�����ѳ����ȼ�ͼ״�����ɲ�ҵ�����Դ�������Դ�����ʣ����ٻ�����Ⱦ������д���пհף�
��l����ⱥ��ʳ��ˮʱ���ܷ�Ӧ�����ӷ���ʽ�� ��
��2��д���������Ȼ����õ����Ȼ��ѵĻ�ѧ���� ��
��3����֪����Mg(s)+ Cl2(g)��MgCl2(s) ��H=��641kJ��mol-1
��Ti(s)+ 2Cl2(g)��TiCl4(s) ��H= ��770kJ��mol-1
��2Mg(s)+ TiCl4(s)��2MgCl2(s) + Ti(s) ��H�� ��
��Ӧ2Mg(s)+ TiCl4(s)![]() 2MgCl2(s)+ Ti����Ar�����н��е������ǣ� ______________________________________ ��
2MgCl2(s)+ Ti����Ar�����н��е������ǣ� ______________________________________ ��
��4���Լ״�������������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�ء��õ���и����ϵĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��ɽ��ʡ������ѧ�߿�����ģ�����⣨���������ۺϻ�ѧ�Ծ����������� ���ͣ������
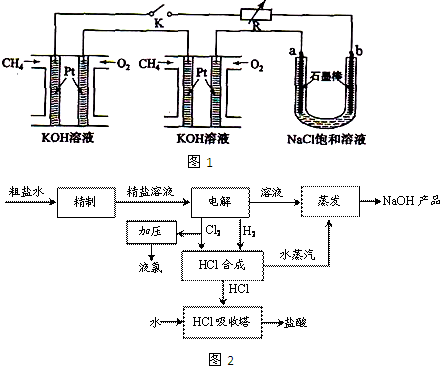
��15�֣��ѣ�Ti������Ϊ��������֮��ĵ�������������ͼ��ʾ�����ѳ����ȼ�ͼ״�����ɲ�ҵ�����Դ�������Դ�����ʣ���С������Ⱦ������д���пհף�
��1����ⱥ��ʳ��ˮʱ���÷�Ӧ�����ӷ���ʽ��____________________��
��2����֪����Mg(s)��Cl2(g)=MgCl2(s);
��

�� ____________
____________
��Ӧ��

 ��Ar������������________
��Ar������������________
��3��д���������뽹̿��Cl2�����Ƶ����Ȼ��ѵĻ�ѧ����ʽ______________________
��4���Լ״�������������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�ء���֪��ȼ�ϵ�ص��ܷ�ӦʽΪ��2CH3OH��3O2��4OH��=2CO32����6H2O����ȼ�ϵ�ط�����Ӧʱ��������Һ��PH_____�����������С�����䡱���õ���и����ϵĵ缫��Ӧ��__________.
��5����������ҵ���кϳ�96t�״�����������H2_________t���������������������ʵ��κ���ʧ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com