
分析 同温同压下,体积相同,据n=$\frac{V}{Vm}$,则n相同,1mol烃CxHy耗氧量为(x+$\frac{y}{4}$)mol;等质量的烃完全燃烧,碳元素质量分数越大,生成二氧化碳越大.
解答 解:同温同压下,体积相同,据n=$\frac{V}{Vm}$,则n相同,设CH4、C2H4、C2H6的物质的量为1mol,1molCH4的耗氧量为(1+1)mol=2mol,1molC2H4的耗氧量为(2+1)mol=3mol,1molC2H6的耗氧量为(2+$\frac{6}{4}$)=3.5mol,故需要的氧气最多的是C2H6;CH4中C、H原子数目之比为1:4,C2H4中C、H原子数目之比为1:2,C2H6中C、H原子数目之比为1:3,故碳元素质量分数CH4<C2H6<C2H4,等质量的烃完全燃烧,碳元素质量分数越大,生成二氧化碳越大,故C2H4生成二氧化碳最多,
故答案为:C2H6;C2H4.
点评 本题考查烃燃烧有关计算,难度不大,注意根据烃燃烧通式及H元素质量分数理解耗氧量问题.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 镁用于制造轻合金,是制造飞机、火箭的重要材料 | |
| B. | 高纯度硅制成的光电池,可用作火星探测器的动力 | |
| C. | 聚脂纤维属于新型无机非金属材料,可制作宇航服 | |
| D. | 高温结构陶瓷耐高温、耐氧化,是喷气发动机的理想材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
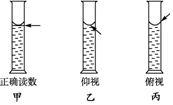 在配制一定物质的量浓度溶液的实验中,用量筒去取用一定量的浓溶液.量液时,量筒必须放平,视线要跟量筒内液体的凹液面最低点保持水平(如图甲),再读出液体的体积数.
在配制一定物质的量浓度溶液的实验中,用量筒去取用一定量的浓溶液.量液时,量筒必须放平,视线要跟量筒内液体的凹液面最低点保持水平(如图甲),再读出液体的体积数.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
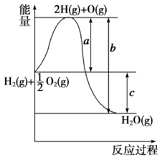 已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g),反应过程中能量变化如图所示,则:
已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g),反应过程中能量变化如图所示,则:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
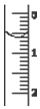 现使用酸碱中和滴定法测定市售白醋的总酸量(g•100mL-1).
现使用酸碱中和滴定法测定市售白醋的总酸量(g•100mL-1).| 滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+、Cu2+、Sb3+ | B. | Cu2+、Ag+、Sb3+ | C. | Sb3+、Ag+、Cu2+ | D. | Ag+、Sb3+、Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com