
| A�� | �ִ���ѧԪ�ط��������У�����Ԫ�ط�����ȷ���������Ƿ���C��H��O��N��S��Cl��Br��Ԫ�أ��ú��������ȷ���������Ƿ����ijЩ�л�ԭ���ţ���ԭ�����չ���ȷ�������к�����Щ����Ԫ�ص� | |
| B�� | �ƼغϽ��ڳ�������Һ�壬�����ڿ����ӷ�Ӧ��������þ�Ͻ���������������������ͷɻ��IJ����� | |
| C�� | 2015���㽭ʡ������������������б�������������������β��ռ20%���ϣ�һ������β���е���Ҫ��Ⱦ��ΪNOx��CO��ȼ��Դ��ϸ������PM2.5�����к����ʣ�����PM2.5��OM��λΪ�����֮һ�ף�������СԼ���ڽ������� | |
| D�� | ��ͼ��ʾΪ�Ĵ������Ӧ�����ϵ����Ӧ4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��������3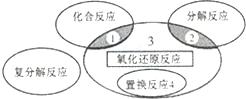 |
���� A��Ԫ�ط����ǿ�ȷ��Ԫ�ص����ࣻ��������ǿ�ȷ�����ۼ��Լ�ԭ���ţ�ԭ�����չ���ȷ������Ԫ�����ࣻ
B���ƼغϽ��۵�ͣ�������ǿ��þ�Ͻ��ܶ�С��Ӳ�ȴ�
C��PM2.5��ָ������ֱ��С�ڻ����2.5�Ŀ����
D.4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O����������ԭ��Ӧ�������������ֻ�����Ӧ���ͣ�
��� �⣺A��Ԫ�ط�������Ϊһ��ʵ���ҳ�����������ͬʱ���л��Ĺ��塢�ӷ��Ժ�������������C��H��N��S��Ԫ�صĺ������ж��������ⶨ��������������������ʶԲ�ͬ�����ĺ��������������ԣ����з��ӽṹ�ͻ�ѧ��ɷ������������ú�������ǿ���ȷ���������Ƿ����ijЩ�л�ԭ�ӻ��ţ�ԭ�����չ������ǻ��������������б���Ԫ�صĻ�̬ԭ�Ӷ��ɹ�Դ�����ĸ�ԭ�ӵ�������խƵ��������������գ����������һ����Χ�����������б���Ԫ�صĻ�̬ԭ��Ũ�ȳ����ȣ��Դ˲ⶨ�����и�Ԫ�غ�����һ����������������������ȷ�������к�����Щ����Ԫ�أ���A��ȷ��
B���ƼغϽ��۵�ͣ�������ǿ�������ڿ����ӷ�Ӧ��������þ�Ͻ��ܶ�С��Ӳ�ȴ������������������ͷɻ��IJ����ȣ���B��ȷ��
C��PM2.5��ָ������ֱ��С�ڻ����2.5�Ŀ�����������ӵ�ֱ����1-100nm֮�䣬PM2.5�ڴ�С�ϰ����������ӣ���C����
D.4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O����������ԭ��Ӧ�������������ֻ�����Ӧ���ͣ���D��ȷ��
��ѡC��
���� ���⿼���Ϊ�ۺϣ��漰���ʵļ��鷽�����Ͻ𡢴�����Ⱦ�Լ���Ӧ���͵�֪ʶ��Ϊ�߿��������ͣ������ڻ�ѧ����������Ŀ��飬����������ѧ�����õĿ�ѧ���������ѧϰ�Ļ����ԣ�ע����ػ���֪ʶ�Ļ��ۣ��ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu��NO3��2��KOH | B�� | Ca��ClO��2��Na2CO3 | C�� | ��NH4��2SO4��BaCl2 | D�� | K2SO4��Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
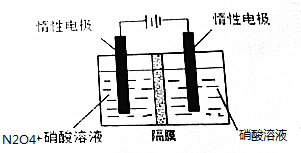
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ����Ϊˮ���Ĵ���� | |
| B�� | �ö�����̼��ȫ�������ϣ����Ի�������ЧӦ | |
| C�� | �������մɺ��ά���������ǽ������� | |
| D�� | ���飨C3H8�����Ҵ���C2H5OH��������ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO 2���ӱ���ģ�ͣ� | B�� | S 2-�Ľṹʾ��ͼ�� | ||
| C�� | ������Ϊ20����ԭ�ӣ�${\;}_{17}^{20}$Cl | D�� | HCN���ӵĽṹʽ��H-C��N |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ | B�� | �������ڼ��� | ||
| C�� | SiO2�������������� | D�� | NaHCO3�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol/L KNO3��Һ����H+��Fe2+��Al3+��Cl- | |
| B�� | ������Һ��NH4+��Fe2+��K+��SO42- | |
| C�� | ������Һ��ClO-��SO32-��K+��Na+ | |
| D�� | ������Ӧ����������������Һ��K+��Cl-��CO32-��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢ۢ� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| Ũ��/mol•L-1 | 4��10-6 | 6��10-4 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com