解:(1)根据质量守恒定律及题干信息可知,反应物是NaNO
2和NH
4Cl,生成物是N
2和H
2O和NaCl,用观察法配平即可,反应方程式为:NH
4Cl+NaNO
2
NaCl+N
2↑+2H
2O,故答案为:NH
4Cl+NaNO
2
NaCl+N
2↑+2H
2O;
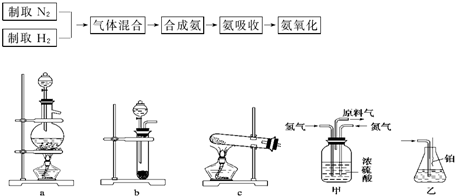
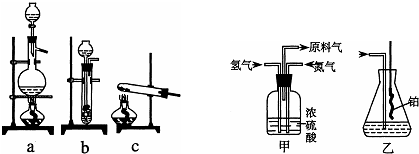
(2)甲装置的作用有将气体混合均匀、控制氢气和氮气的流速、干燥气体,
故答案为:干燥气体,观察气泡速度,控制氢气和氮气的流速;
(3)氨气的混合气体中含有大量的氮气和氢气,均是难溶于水的气体,不会倒吸,
故答案为:不会;混合气体中含有大量难溶于水的氮气和氢气;
(4)氨的氧化反应是一个放热反应,放出的热使铂丝保持红热,生成的一氧化氮与空气中的氧气化合成二氧化氮,二氧化氮是红棕色气体,故答案为:氨的氧化反应是一个放热反应,放出的热使铂丝保持红热;有红棕色气体产生;
(5)氨的催化氧化反应方程式为:4NH
3+5O
2
4NO+6H
2O,故答案为:4NH
3+5O
2
4NO+6H
2O;
(6)已知①CH
4(g)+4N0
2(g)═4NO(g)+C0
2(g)+2H
20(g)△H=-574kJ?mol
-1,
②CH
4(g)+4N0(g)═2N
2(g)+C0
2(g)+2H
20(g)△H=-1160kJ?mol
-1,
则反应CH
4(g)+2N0
2(g)═N
2(g)+C0
2(g)+2H
20(g)等于

(①+②),
根据盖斯定律,所以反应CH
4(g)+2N0
2(g)═N
2(g)+C0
2(g)+2H
20(g)△H=

[(-574kJ?mol
-1)+(-1160kJ?mol
-1)]=-867KJ/mol,反应CH
4(g)+2N0
2(g)═N
2(g)+C0
2(g)+2H
20(g)中,1mol甲烷参加反应转移电子数为8mol,所以标准状况下4.48L极0.2molCH
4还原NO
2至N
2整个过程中转移的电子为1.6mol,电子总数为1.6N
A,当转移8mol电子,放出的能量为867KJ,所以转移1.6mol电子放出的能量为173.4KJ,
故答案为:CH
4(g)+2N0
2(g)═N
2(g)+C0
2(g)+2H
20(g)△H=-867KJ/mol;1.6N
A;173.4.
分析:(1)根据题干信息可知:反应物是NaNO
2和NH
4Cl,有N
2生成,反应中只有氮元素发生变价,结合质量守恒定律可知:生成物还有NaCl和H
2O,然后进行配平即可,注意反应条件;
(2)甲装置的作用有将气体混合均匀、控制氢气和氮气的流速、干燥气体;
(3)混合气体中含有大量的氮气和氢气,均是难溶于水的气体,极易溶于水的气体易发生倒吸;
(4)氨的氧化反应是一个放热反应;生成的一氧化氮与空气中的氧气化合成二氧化氮;
(5)根据氨气的化学性质来回答;
(6)根据盖斯定律来计算反应的焓变,并根据化合价的升降来判断电子转移情况,计算反应热的多少.
点评:本题以信息形式主要考查了氮气的制取、以及氮的化合物的性质,综合性较大,旨在考查学生对知识的迁移运用,依据已有的知识进行.


 NaCl+N2↑+2H2O,故答案为:NH4Cl+NaNO2
NaCl+N2↑+2H2O,故答案为:NH4Cl+NaNO2 NaCl+N2↑+2H2O;
NaCl+N2↑+2H2O; 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2 4NO+6H2O;
4NO+6H2O; (①+②),
(①+②), [(-574kJ?mol-1)+(-1160kJ?mol-1)]=-867KJ/mol,反应CH4(g)+2N02(g)═N2(g)+C02(g)+2H20(g)中,1mol甲烷参加反应转移电子数为8mol,所以标准状况下4.48L极0.2molCH4还原NO2至N2整个过程中转移的电子为1.6mol,电子总数为1.6NA,当转移8mol电子,放出的能量为867KJ,所以转移1.6mol电子放出的能量为173.4KJ,
[(-574kJ?mol-1)+(-1160kJ?mol-1)]=-867KJ/mol,反应CH4(g)+2N02(g)═N2(g)+C02(g)+2H20(g)中,1mol甲烷参加反应转移电子数为8mol,所以标准状况下4.48L极0.2molCH4还原NO2至N2整个过程中转移的电子为1.6mol,电子总数为1.6NA,当转移8mol电子,放出的能量为867KJ,所以转移1.6mol电子放出的能量为173.4KJ,

 阅读快车系列答案
阅读快车系列答案