
实验题(17分)工业上可用下列仪器组装一套装置来测定黄铁矿中硫的质量分数(忽悠SO2、H2SO3与氧气的反应)。
实验的正确操作步骤如下:
A、连接好装置,并检查装置的气密性
B、称取研细的黄铁矿样品
C、将2.0g样品小心地放入硬质玻璃管中。
D、以1L/min的速率不断鼓入空气。
E、将硬质玻璃管中的黄铁矿样品加热到800℃~850℃。
F、用300ml的饱和碘水吸收SO2 ,发生的反应是:I2+SO2+2H2O=H2SO4+2HI
G、吸收液用CCl4萃取,分离得到上层无色溶液
H、取20.00ml 吸收液,用标准0.2000 mol·L-1的NaOH溶液滴定。(填“上”、“下”)层溶液进行后续实验。
试回答:
(1) 步骤G中所有主要仪器是 、应取
(2)装置⑤的作用是 ;
(3) 装置连接顺序是 (填编号)。
(4) 步骤H中滴定时应选用 作指示剂,可以根据 现象判断滴定已达到终点。
(5) 假定黄铁矿中的硫在操作E中已全部转化为SO2,并全部饱和碘水完全吸收。滴定得到的数据如表所示:
|
滴定次数 |
待测液的体积/mL |
标准溶液NaOH(aq)体积 |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
第一次 |
20.00mL |
0.00 |
20.48 |
|
第二次 |
20.00mL |
0.22 |
22.15 |
|
第三次 |
20.00mL |
0.36 |
20.38 |
则该黄铁矿样品中硫元素的质量分数为 。(保留小数点后1位)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.用于合成氨的工业煤气中含有H2S、C2H5SH(乙酸醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理。
H2S+ZnO=ZnS+H2O;C2H5SH+ZnO=ZnS+C2H4+H2O
C2H5SH+H2=C2H6+H2S;COS+H2=CO+H2S;CS2+4H2=CH4+2H2S
(1)钴原子在基态时核外电子排布式为 。
(2)下列有关分子结构的说法正确的是 。
A.C2H4分子中有5个![]() 键处1个
键处1个![]() 键
键
B.COS分子(结构如右图)中键能C=O>C=S
C.H2S分子呈V形结构
D.CH4、C2H6分子中碳原子均采用sp3杂化
(3)下列有关说法不正确的是 。
A.H2O、CO、COS均是极性分子
B.相同压强下沸点:Cs2>COS>CO2
C.相同压强下沸点:C2H5SH>C2H5OH
D.相同压强下沸点:CO>N2
(4)![]() -ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
-ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于 。
(6)钼的一种配合物化学式为:Na3[Mo(CN)8]·8H2O,中心原子的配位数为 。
B.烃醛结合反应有机合成中颇为重要,绿色催化剂的固体铌酸酸倍受研究者关注。铌酸具有较高的催化活性及稳定性。反应原理如下:
实验方法是在25mL烧瓶中加入铌酸、10mL甲醇和 0.5mL苯甲醛,在回流状态下反应2h,反应的产率和转化率均非常高。
(1)采用回流反应2h的目的是 。
(2)在反应中甲醇需过量,其原因是 。
(3)不同铌酸用量对产率和转化率影响,如下表:
| 铌酸用量/mol | 0.01 | 0.02 | 0.03 | 0.05 | 0.1 | 0.15 | 0.2 | 0.6 |
| 产率% | 87.3 | 88.2 | 90.3 | 94.2 | 92.9 | 93.1 | 91.8 | 92.3 |
| 转化率% | 89.7 | 92.1 | 93.9 | 98.9 | 94.9 | 95.7 | 93.9 | 94.3 |
在上述苯甲醛与甲醇缩合反应实验中催化剂铌酸的最佳用量为 。
(4)催化剂的回收利用性能是考察催化剂的一项极为重要的指标。铌酸催化剂循环使用次数对产率的影响如右下图,这说明铌酸催化剂的优点之一是 。
(5)用铌酸作催化剂时,不同的醛与甲醇的缩合反应的转化率和产率如下表:
| 序号 | 醛 | 醇 | 转化率% | 产率% |
| 1 | 邻羟基苯甲醛 | 甲醇 | 94.3 | 89.6 |
| 2 | 邻羟基苯甲醛 | 甲醇 | 93.6 | 88.7 |
| 3 | 邻氯苯甲醛 | 甲醇 | 93.1 | 87.3 |
| 4 | 间硝基苯甲醛 | 甲醇 | 54.2 | 34.1 |
| 5 | 邻硝基苯甲醛 | 甲醇 | 89.9 | 79.5 |
| 6 | 对硝基苯甲醛 | 甲醇 | 65.7 | 41.9 |
从表中得出的不同的醛与甲醇缩合反应影响转化率和产率的规律是 。
查看答案和解析>>
科目:高中化学 来源:2010年江苏省盐城市高三上学期摸底考试化学试题 题型:填空题
(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.用于合成氨的工业煤气中含有H2S、C2H5SH(乙酸醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理。
H2S+ZnO=ZnS+H2O;C2H5SH+ZnO=ZnS+C2H4+H2O
C2H5SH+H2=C2H6+H2S;COS+H2=CO+H2S;CS2+4H2=CH4+2H2S
(1)钴原子在基态时核外电子排布式为 。
(2)下列有关分子结构的说法正确的是 。
A.C2H4分子中有5个 键处1个
键处1个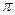 键
键
B.COS分子(结构如右图)中键能C=O>C=S
C.H2S分子呈V形结构
D.CH4、C2H6分子中碳原子均采用sp3杂化
(3)下列有关说法不正确的是 。
A.H2O、CO、COS均是极性分子
B.相同压强下沸点:Cs2>COS >CO2
>CO2
C.相同压强下沸点:C2H 5SH>C2H5OH
5SH>C2H5OH
D.相同压强下沸点:CO>N2
(4) -ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
-ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于 。
(6)钼的一种配合物化学式为:Na3[Mo(CN)8]·8H2O,中心原子的配位数为 。
B.烃醛结合反应有机合成中颇为重要,绿色催化剂的固体铌酸酸倍受研究者关注。铌酸具有较高的催化活性及稳定性。反应原理如下:
实验方法是在25mL烧瓶中加入铌酸、10mL甲醇和 0.5mL苯甲醛,在回流状态下反应2h,反应的产率和转化率均非常高。
(1)采用回流反应2h的目的是 。
(2)在反应中甲醇需过量,其原因是 。 (3)不同铌酸用量对产率和转化率影响,如下表:
(3)不同铌酸用量对产率和转化率影响,如下表:
| 铌酸用量/mol | 0.01 | 0.02 | 0.03 | 0.05 | 0.1 | 0.15 | 0.2 | 0.6 |
| 产率% | 87.3 | 88.2 | 90.3 | 94.2 | 92.9 | 93.1 | 91.8 | 92.3 |
| 转化率% | 89.7 | 92.1 | 93.9 | 98.9 | 94.9 | 95.7 | 93.9 | 94.3 |
| 序号 | 醛 | 醇 | 转化率% | 产率% |
| 1 | 邻羟基苯甲醛 | 甲醇 | 94.3 | 89.6 |
| 2 | 邻羟基苯甲醛 | 甲醇 | 93.6 | 88.7 |
| 3 | 邻氯苯甲醛 | 甲醇 | 93.1 | 87.3 |
| 4 | 间硝基苯甲醛 | 甲醇 | 54.2 | 34.1 |
| 5 | 邻硝基苯甲醛 | 甲醇 | 89.9 | 79.5 |
| 6 | 对硝基苯甲醛 | 甲醇 | 65.7 | 41.9 |

查看答案和解析>>
科目:高中化学 来源:2010年江苏省盐城市高三上学期摸底考试化学试题 题型:填空题
(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.用于合成氨的工业煤气中含有H2S、C2H5SH(乙酸醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理。
H2S+ZnO=ZnS+H2O;C2H5SH+ZnO=ZnS+C2H4+H2O
C2H5SH+H2=C2H6+H2S;COS+H2=CO+H2S;CS2+4H2=CH4+2H2S
(1)钴原子在基态时核外电子排布式为 。
(2)下列有关分子结构的说法正确的是 。
A.C2H4分子中有5个 键处1个
键处1个 键
键
B.COS分子(结构如右图)中键能C=O>C=S
C.H2S分子呈V形结构
D.CH4、C2H6分子中碳原子均采用sp3杂化
(3)下列有关说法不正确的是 。
A.H2O、CO、COS均是极性分子
B.相同压强下沸点:Cs2>COS>CO2
C.相同压强下沸点:C2H5SH>C2H5OH
D.相同压强下沸点:CO>N2
(4)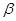 -ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
-ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。

(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于 。
(6)钼的一种配合物化学式为:Na3[Mo(CN)8]·8H2O,中心原子的配位数为 。
B.烃醛结合反应有机合成中颇为重要,绿色催化剂的固体铌酸酸倍受研究者关注。铌酸具有较高的催化活性及稳定性。反应原理如下:

实验方法是在25mL烧瓶中加入铌酸、10mL甲醇和 0.5mL苯甲醛,在回流状态下反应2h,反应的产率和转化率均非常高。
(1)采用回流反应2h的目的是 。
(2)在反应中甲醇需过量,其原因是 。
(3)不同铌酸用量对产率和转化率影响,如下表:
|
铌酸用量/mol |
0.01 |
0.02 |
0.03 |
0.05 |
0.1 |
0.15 |
0.2 |
0.6 |
|
产率% |
87.3 |
88.2 |
90.3 |
94.2 |
92.9 |
93.1 |
91.8 |
92.3 |
|
转化率% |
89.7 |
92.1 |
93.9 |
98.9[来源:Zxxk.Com] |
94.9 |
95.7 |
93.9 |
94.3 |
在上述苯甲醛与甲醇缩合反应实验中催化剂铌酸的最佳用量为 。
(4)催化剂的回收利用性能是考察催化剂的一项极为重要的指标。铌酸催化剂循环使用次数对产率的影响如右下图,这说明铌酸催化剂的优点之一是 。
(5)用铌酸作催化剂时,不同的醛与甲醇的缩合反应的转化率和产率如下表:
|
序号 |
醛 |
醇 |
转化率% |
产率% |
|
1 |
邻羟基苯甲醛 |
甲醇 |
94.3 |
89.6 |
|
2 |
邻羟基苯甲醛 |
甲醇 |
93.6 |
88.7 |
|
3 |
邻氯苯甲醛 |
甲醇 |
93.1 |
87.3 |
|
4 |
间硝基苯甲醛 |
甲醇 |
54.2 |
34.1 |
|
5 |
邻硝基苯甲醛 |
甲醇 |
89.9 |
79.5 |
|
6 |
对硝基苯甲醛 |
甲醇 |
65.7 |
41.9 |

从表中得出的不同的醛与甲醇缩合反应影响转化率和产率的规律是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验题(17分)工业上可用下列仪器组装一套装置来测定黄铁矿中硫的质量分数(忽悠SO2、H2SO3与氧气的反应)。
实验的正确操作步骤如下:
A、连接好装置,并检查装置的气密性
B、称取研细的黄铁矿样品
C、将2.0g样品小心地放入硬质玻璃管中。
D、以1L/min的速率不断鼓入空气。
E、将硬质玻璃管中的黄铁矿样品加热到800℃~850℃。
F、用300ml的饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O=H2SO4+2HI
G、吸收液用CCl4萃取,分离得到上层无色溶液
H、取20.00ml 吸收液,用标准0.2000mol·L-1的NaOH溶液滴定。(填“上”、“下”)层溶液进行后续实验。
试回答:
(1) 步骤G中所有主要仪器是 、应取
(2)装置⑤的作用是 ;
(3) 装置连接顺序是 (填编号)。
(4) 步骤H中滴定时应选用 作指示剂,可以根据 现象判断滴定已达到终点。
(5) 假定黄铁矿中的硫在操作E中已全部转化为SO2,并全部饱和碘水完全吸收。滴定得到的数据如表所示:
| 滴定次数 | 待测液的体积/mL | 标准溶液NaOH(aq)体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 第一次 | 20.00mL | 0.00 | 20.48 |
| 第二次 | 20.00mL | 0.22 | 22.15 |
| 第三次 | 20.00mL | 0.36 | 20.38 |
则该黄铁矿样品中硫元素的质量分数为 。(保留小数点后1位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com