
| A. | 苯(甲苯)KMnO4(酸化),NaOH溶液分液 | B. | 乙烷(乙烯)酸性KMnO4(溶液洗气 | ||
| C. | 乙酸乙酯(乙酸)KOH溶液分液 | D. | 苯(苯酚)浓Br2水过滤 |
分析 A.甲苯能被高锰酸钾氧化,而苯不能,且苯甲酸与NaOH反应后与苯分层;
B.乙烯被高锰酸钾氧化生成二氧化碳;
C.二者均与KOH反应;
D.溴易溶于苯、生成的三溴苯酚易溶于苯.
解答 解:A.甲苯能被高锰酸钾氧化,而苯不能,且苯甲酸与NaOH反应后与苯分层,然后分液可分离,故A正确;
B.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,不能除杂,应选溴水、洗气,故B错误;
C.二者均与KOH反应,不能除杂,应选饱和碳酸钠溶液、分液,故C错误;
D.溴易溶于苯、生成的三溴苯酚易溶于苯,不能除杂,应选NaOH、分液,故D错误;
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意有机物性质的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 5.6 g Fe 和足量的氧气完全燃烧失去电子数为 3N A | |
| B. | 1L 浓度为 0.5mol/LFeCl3 溶液加热煮沸后,会生成 0.5molFe(OH)3胶体粒子 | |
| C. | 常温常压下,23 g NO2 和 N2O4 的混合气体一定含有 N A 个氧原子 | |
| D. | 标况下,4.48L 的水中含有 H2O 分子的数目为 0.2N A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
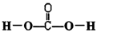 .
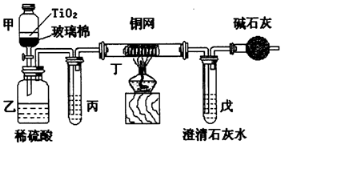
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
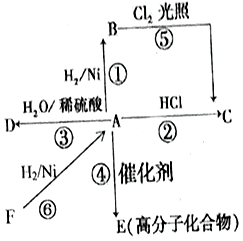 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者都能溶于水并且都能和水反应,前者的溶解度大于后者 | |
| B. | 两者都能用于治疗胃酸过多疾病,前者的效果好于后者 | |
| C. | 足量的Na2CO3和NaHCO3分别与等物质的量的稀盐酸反应,前者产生CO2多 | |
| D. | 等体积等浓度的AlCl3溶液分别和足量的Na2CO3和NaHCO3反应,前者产生CO2多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠燃烧,可用砂子灭火,不能用二氧化碳灭火器来灭火 | |
| B. | 眼睛里不慎溅进了稀药液,应立即用水冲洗,并且用手使劲揉眼睛 | |
| C. | 少量浓硫酸沾到皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 熄灭酒精灯可直接用嘴吹 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com