
有一分子式为C5H10N2O3的二肽,经水解得到甘氨酸(氨基乙酸)和另一种氨基酸X,则X的分子式为( )
A.C3H7NO2 B.C3H8NO3 C.C3H7N2O2 D.C3H8NO3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐(BrO3-)”这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(Br-),在后续的生产过程中经臭氧(O3)处理逐渐转化成溴酸盐。下列有关该转化过程的认识正确的是( )
A.该过程中溴化物(Br-)得到电子
B.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂
C.该过程中溴元素被还原,氧元素被氧化
D.该过程中溴元素发生氧化反应,氧元素发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验设计和操作中必须十分重视安全问题和环境保护问题,下列实验的设计或操作不合理的是
①实验室用加热分解KClO3的方法制取O2,排水收集O2后,先停止加热,再拆除实验装置。
②实验结束后,应将固体残渣深埋入土壤中,废液倒入下水道排除
③给试管中的液体加热时应不时移动试管,以免暴沸伤人
④为检验CO气体的纯度,用排空气法收集一试管气体,然后移近酒精灯火焰点燃,听有无尖锐爆鸣声
A.①② B.①②③④ C.①②④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,下列有关说法不正确的是
A.产物乙酸乙酯存在18O B.产物水中存在18O
C.反应中加入浓硫酸作催化剂 D.此反应属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ·mol-1;
②2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1。
则制备水煤气的反应C(s)+H2O(g) ===CO(g)+H2(g)的ΔH为( )
A.262.6 kJ·mol-1 B.-131.3 kJ·mol-1
C.-352.3 kJ·mol-1 D.131.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构为下图所示,这种有机物不可能具有的性质是( )
①可以燃烧; ②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应; ⑥能发生水解反应
A.①④ B.只有⑥ C.只有⑤ D.④⑥
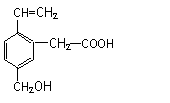
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)中和热的测定是高中化学的定量实验之一.50 mL0.50 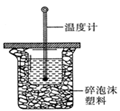 mol/L 盐酸与50 mL
mol/L 盐酸与50 mL
0.55 mol/L NaOH 溶液在如图所示的装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。从实验
装置上看,图中尚缺少的一种仪器是 。大烧杯上如不
盖硬纸板,求得的中和热数值将会
(填“偏大”、“偏小”或“无影响”)。
(2)氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越
越多的关注。
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的
影响。在常温下按照下表所示的方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是________。
同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条
件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法
 是 ________(填一种即可)。
是 ________(填一种即可)。
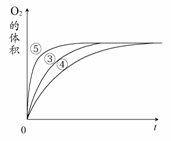
(2)实验③④⑤中,测得生成氧气的体积随时间变化
的关系右图所示。
分析该图能够得出的实验结论是________。
Ⅱ.资料显示,某些金属离子对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2
分解的催化效果,该实验小组的同学设计了如图所示的实验装置进行实验。
(1)某同学通过测定O2的体积比较H2O2的分解速率快慢,实验时可以通过测量
________ 或 ________比较;
(2)0.1g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时
间的关系如图所示。解释反应速率变化的原因:________,计算H2O2的初始物
质的量浓度为________。(保留两位有效数字,在标准状况下测定)
Ⅲ.(1)为了加深对影响反应速率因素的认识,老师让甲同学完成下列实验:
在Ⅱ中的实验装置的锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分液
漏斗加入40 mL 2.5 mol/L的硫酸,10s时收集产生的H2体积为50 mL
(若折合成标准状况下的H2体积为44.8mL),用锌粒表示10s内该反应的速
率为______g/s;
(2)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法
不正确的是________(填序号)。
A.化学反应速率理论可以指导怎样在一定时间内快出产品
B.勒夏特列原理可以指导怎样使有限原料多出产品
C.催化剂的使用是提高原料转化率的有效办法
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源: 题型:
为了检验氯乙烷中含氯元素,试从①~⑥各步实验操作中,必要的实验操作及合理的顺序是:①加热;②加入蒸馏水;③加入硝酸银溶液;④加入氢氧化钠溶液⑤加入氢氧化钠的醇溶液;⑥加入硝酸溶液。
A.④①⑥③ B.②①③⑥ C.⑤①③⑥ D.①④③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com