
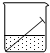
| A. | 铁钉与水面交接处最易腐蚀 | |
| B. | 铁钉发生吸氧腐蚀,铁做阴极 | |
| C. | 铁发生的反应是:Fe-3e→Fe3+ | |
| D. | 水上和水下部分的铁钉不发生电化腐蚀 |
分析 将铁钉放入纯水中,由于铁钉为铁的合金,含有碳单质,故在纯水做电解质溶液的环境下,铁做负极,碳做正极,中性的水做电解质溶液,发生钢铁的吸氧腐蚀,据此分析.
解答 解:A、在铁钉和水面的交界处,有水做电解质溶液,氧气的浓度最高,故发生吸氧腐蚀的速率最大,则最易被腐蚀,故A正确;
B、由于水为中性,故钢铁发生吸氧腐蚀,其中铁做负极,故B错误;
C、铁做负极,电极反应为:Fe-2e→Fe2+,故C错误;
D、由于水的蒸发,故在铁钉的水面以上的部分上仍然有水膜,仍然能发生吸氧腐蚀;由于氧气能溶解在水中,故铁钉水面一下的部分也能发生吸氧腐蚀,但均没有铁钉和水的交接处的腐蚀速率大,故D错误.
故选A.
点评 本题考查了钢铁的吸氧腐蚀,难度不大,应注意无论是钢铁的吸氧腐蚀还是析氢腐蚀,负极反应均为Fe-2e→Fe2+.


科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:Fe2+>Fe3+ | |
| B. | 酸性:HClO4>H2SO4>H2SeO4 | |
| C. | 反应活泼性:O>03>02 | |
| D. | 物质的量浓度:pH相等时,CH3C00H>HCl0. |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH2=CH2和HCHO都能使溴水褪色 | |
| B. | CH4和苯都能够和氯单质发生反应 | |
| C. | 卤代烃与氢氧化钠水溶液或醇溶液发生反应 | |
| D. | 二氧化硫能使溴水或者酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
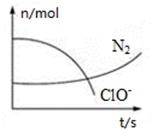 某反应体系中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种微粒,反应过程中测得ClO-和N2的物质的量随时间的变化如图所示.有关判断正确的是( )
某反应体系中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种微粒,反应过程中测得ClO-和N2的物质的量随时间的变化如图所示.有关判断正确的是( )| A. | 氧化剂是ClO-,还原产物是HCO3- | |
| B. | 反应体系中反应物与生成物各有三种微粒 | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 生成2.24L N2(标准状况)时转移电子0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三者的氧化物都是碱性氧化物 | |
| B. | 三者的氢氧化物都是白色固体 | |
| C. | 三者的氯化物都可用化合反应制得 | |
| D. | 三者的单质在空气中最终都生成氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2.4g | B. | 4.8g | C. | 6g | D. | 6.18g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成氨使用高压 | B. | 制硝酸用Pt-Rh合金作催化剂 | ||
| C. | 制硫酸时接触室使用较高温度 | D. | 侯氏制碱法循环利用母液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 当滴入20mL NaOH溶液时:2c(SO42-)=c(NH3•H2O)+c(NH4+) | |
| B. | 当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| C. | 当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)=c(OH-) | |
| D. | 整个反应过程中:c(H+)+c(Na+)+c(NH4+)=c(OH-)+2c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上用FeCl3溶液吸收废气中的H2S气体,离子方程式为:Fe3++H2S=Fe2++S↓+2H+ | |
| B. | 在0.1 mol/L的AlCl3溶液中,Na+、K+、SO42-、HCO3-均可大量共存 | |
| C. | 常温下pH=4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-) | |
| D. | 已知25℃时NH4CN溶液显碱性,则25℃时的电离平衡常数K(NH3•H2O)>K(HCN) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com