
【题目】根据如图填空:
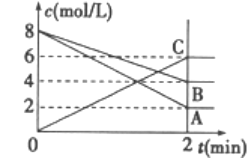
(1)反应物是______________,生成物是______________。
(2)在2 min内用A、B、C表示的化学反应速率分别为____________、____________、____________。
(3)该反应的化学方程式是____________________________。
【答案】A、B C 3 mol/(L·min) 2 mol/(L·min) 3 mol/(L·min) 3A+2B![]() 3C
3C
【解析】
(1)由图像的变化可知A、B的浓度是减小的,而C的浓度是增加的,则反应物为A、B,生成物为C,故答案为:A、B;C。(2)在2min内有ν(A)=(8-2)mol/L÷2min=3 mol/(L·min),ν(B)=(8-4)mol/L÷2min=2 mol/(L·min),ν(C)=6mol/L÷2min=3 mol/(L·min),故答案为:3 mol/(L·min)、2 mol/(L·min)、3 mol/(L·min);(3)由于反应进行2min后处于平衡状态,则反应为可逆反应,且ν(A):ν(B):ν(C)=3:2:3,则方程式中A、B、C三种物质前的系数依次为3、2、3,故答案为:3A+2B![]() 3C。
3C。


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5

(1)装置I中产生气体的化学方程式为__________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是_________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。

实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是____________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果____(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 气态氢化物的稳定性:HCl>HF B. 通入CO2可使漂白粉溶液漂白性增强
C. Al(OH)3、Fe(OH)3受热都易分解 D. Na在空气中燃烧会生成Na2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对化学反应限度的叙述,错误的是( )
A. 任何可逆反应在给定条件下的进程都有一定的限度
B. 化学反应达到限度时,正、逆反应速率相等且不为零
C. 化学反应的限度与时间的长短无关
D. 化学反应的限度是不可改变的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应H2(g)+I2(g) ![]() 2HI(g)达到化学平衡状态的标志是( )
2HI(g)达到化学平衡状态的标志是( )
A. 单位时间内生成n mol H2,同时就有n mol HI生成
B. 单位时间内有n mol H2生成,同时就有n mol I2生成
C. 容器内H2的含量不随时间的变化而变化
D. 1个H—H键断裂的同时,有2个H—I键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
活性炭/mol | NO/mol | A/mol | B/mol | |
起始状态 | 2.030 | 0.100 | 0 | 0 |
2 min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2 min内,用NO表示该反应的平均速率v(NO)= mol·L-1·min-1;
(2)该反应的化学方程式是________________________________________;
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_____ 。
①v(NO)∶v(A)∶v(B)=2∶1∶1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O。

①a处通入的物质是____,电极反应式为:______;
②b处电极反应式为_________________________;
③电池工作时H+由 极移向 极(填正、负极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(夹持装置略)、试剂和操作方法有错误的是

A. 观察Fe(OH)2的生成
B. 除去CO中的CO2
C. 配制一定物质的量浓度的NaNO3溶液
D. 25 mL滴定管读数为11.80 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气在氧气中燃烧时产生淡蓝色火焰.在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol O2中的化学键消耗的能量为Q2 kJ,形成1mol H2O中的化学键释放的能量为Q3 kJ.下列关系式中,正确的是
A. Q1+Q2>Q3B. 2Q1+Q2>2Q3
C. 2Q1+Q2<2Q3D. Q1+Q2<2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下有机物:① ![]() ②
② ![]() ③
③ ![]() ④
④ ![]() ⑤苯酚
⑤苯酚
(1)能与Na反应的是 ________ ;
(2)能与![]() 溶液反应的有_________;
溶液反应的有_________;
(3)能与NaHCO3溶液反应有气泡产生的是_______________;
(4)能与银氨溶液发生银镜反应的有____________________;
(5)既能发生消去反应,又能发生酯化反应的有___________________;
(6)能发生氧化反应的有(除燃烧以外)___________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com