
下列对摩尔(mol)的有关说法中错误的是
A.摩尔是一个单位而非物理量
B.摩尔既能用来计量纯净物,又能用来计量混合物
C.1mol任何气体所含气体的分子数目都相等
D.0.5mol氦约含有1.204×1024个电子
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(文)化学试卷(解析版) 题型:选择题
在日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等名词,这里的碘、铁、钙、硒、氟应理解为
A.元素 B.单质 C.分子 D.氧化物
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
可以验证硫元素的非金属性比氯元素弱的事实是
①H2S水溶液是弱酸,HCl水溶液是强酸
②向氢硫酸溶液中滴入氯水有单质硫生成
③硫、氯气分别与铁和铜反应,其产物是FeS、Cu2S、FeCl3、CuCl2
④高氯酸(HClO4)的酸性比硫酸强
A、①②④ B、②④ C、②③④ D、①②③④
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江大庆实验中学高三上学期期中考试化学试卷(解析版) 题型:选择题
向含有下列各离子组的溶液中通入足量相应气体后,各离子还能大量存在的是( )
A.二氧化碳:K+、Na+、SiO32-、Cl-
B.氨气:Ag+、Al3+、Na+、NO3-
C.氯化氢:Ca2+、Fe3+、NO3-、Cl-
D.氯气:Na+、Ba2+、I-、HSO3-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:选择题
在电解水制取H2和O2时,为了增强溶液的导电性,常常要加入一些电解质,最好选用下列物质中的( )
A.HCl B.NA2SO4 C.CuSO4 D.NACl
查看答案和解析>>
科目:高中化学 来源:2016届山西怀仁第一中学高三上学期期中考试化学试卷(解析版) 题型:选择题
二氧化硒( SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。在回收过程中涉及如下化学反应:①SeO2 + 4KI + 4HNO3 =Se + 2I2 + 4KNO3 + 2H2O;②Se + 2H2SO4(浓) = 2SO2↑+ SeO2 + 2H2O;③Se + 4HNO3(浓) = SeO2 + 4NO2↑+ 2H2O。下列有关叙述正确的是
A.SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2
B.反应①中Se是氧化产物,I2是还原产物
C.反应①中生成0.6 mol I2,转移的电子数目为2.4NA
D.反应②、③中等量的Se消耗浓H2SO4和浓HNO3的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源:2015-2016河北石家庄第一中学高一上期中考试化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
A.Fe2O3溶于足量稀盐酸:Fe2O3+6H+=2Fe3++3H2O
B.实验室制CO2:CO32-+2H+=CO2+H2O
C.向澄清石灰水中通入少量CO2:OH-+CO2=HCO3-
D.NaHSO4溶液中加入Ba(OH)2溶液后恰好显中性
Ba2++OH-+H++SO42-=BaSO4+H2O
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期期中考试化学试卷(解析版) 题型:填空题
按下列要求填空:
(1)写出过氧化氢和过氧化钠的电子式: 、 。
(2)已知叠氮酸(HN3)是与醋酸酸性相近的酸。写出其在水溶液中电离的方程式: 。
(3)已知水溶液中,YO3n- 和 3S2- 发生反应,离子方程式如下:YO3n-+3S2-+6H+=Y-+3S↓+3H2O,则微粒YO3n-所带的电荷为 。
(4)写出钢铁吸氧腐蚀中正极的电极反应式: 。
(5)在标准状况下,1L水中能溶解a L氯化氢气体,所得溶液密度为ρg/cm3 。请计算出氢化氢的物 质的量浓度(要求化简) 。
查看答案和解析>>
科目:高中化学 来源:2016届贵州遵义航天高级中学高三第四次模拟考试理化学卷(解析版) 题型:实验题
(14分)某校课外探究小组欲在实验室条件下制取少量纯净的无水氯化铝。查阅到以下资料:无水氯化铝是白色晶体,易吸收水分,常压下在177.8℃升华,遇潮湿空气即产生大量白雾。用于有机合成和石油工业的催化剂,以及用于处理润滑油等。他们设计了以下装置,请结合题意回答问题:
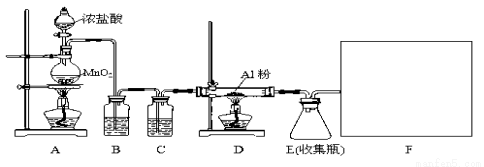
(1)A装置中发生反应的化学方程式为: 。
(2)装置B的作用是 。
(3)请给标记为F的实线方框选择合适的装置 。
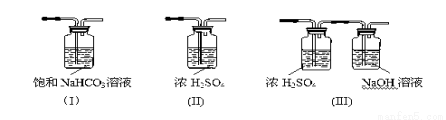
(4)AlCl3遇潮湿空气即产生大量白雾的原因是 (结合化学方程式说明)。
(5)有同学认为装置E中有不足之处,存在安全隐患。若你同意他的观点,请指出其不足之处 。
(6)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,该小组同学提出酸碱中和滴定法测定方案。方案如下:首先准确量取残余清液稀释一定的倍数后作为试样,平行做了4次滴定。实验中所用NaOH溶液浓度为0.2000mol·L-1,以下是实验记录与数据处理(不考虑NaOH与残液中其他成分的反应)。
滴定次数 实验数据ml | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(初读数) | 0.00 | 0.50 | 0.70 | 1.00 |
V(NaOH)终读数) | 22.60 | 22.55 | 22.65 | 23.00 |
①经计算,该次滴定测的试样中盐酸浓度为 mol·L-1。
②在本实验的滴定过程中,下列操作会使实验结果偏小的是 (填写序号)。
a.开始滴定时滴定管尖嘴处留有气泡,滴定结束气泡消失
b.未用标准NaOH溶液润洗滴定管
c.锥形瓶中加入待测盐酸后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前锥形瓶用待测盐酸润洗
f.观察读数时,滴定前仰视,滴定后俯视
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com