
【题目】(1)在一定条件下,体积为2L的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,3min后达到平衡,生成NH3的物质的量是2.4 mol。试求:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,3min后达到平衡,生成NH3的物质的量是2.4 mol。试求:
① 3min内用N2表示的化学反应速率为____________。②H2的转化率是____________。
(2)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。

a.实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子物质的量为____________;
MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子物质的量为____________;
b.①反应开始一段时间后,观察到D试管中的品红溶液出现的现象是:
D:_____________________________________________________________。
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:
B:____________________________________,D:________________________________。
c.另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_______________________________。
【答案】 v(N2) =0.2 mol·L-1·min-1 60% 3mol 品红溶液褪色 褪色的品红溶液又恢复成红色 无明显现象 Cl2+SO2+2H2O=2HCl+H2SO4
【解析】(1)因为生成NH3(g)2.4mol,根据反应N2(g)+3H2(g)![]() 2NH3(g)得,反应的N2(g)为1.2mol,反应的H2(g)为3.6mol,所以①3min内用N2表示的化学反应速率为:1.2mol÷2L÷3min=0.2molL-1min-1;②H2的转化率是:3.6mol÷6.0mol×100%=60%。
2NH3(g)得,反应的N2(g)为1.2mol,反应的H2(g)为3.6mol,所以①3min内用N2表示的化学反应速率为:1.2mol÷2L÷3min=0.2molL-1min-1;②H2的转化率是:3.6mol÷6.0mol×100%=60%。
(2)a.在反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中,每有4mol HCl参与反应,被氧化的氯化氢是2mol,即被氧化的氯化氢占参与反应的50%,6 molHCl参加反应被氧化的氯化氢是3mol,转移的物质的量为3mol。
MnCl2+Cl2↑+2H2O中,每有4mol HCl参与反应,被氧化的氯化氢是2mol,即被氧化的氯化氢占参与反应的50%,6 molHCl参加反应被氧化的氯化氢是3mol,转移的物质的量为3mol。
b.SO2具有漂白性,二氧化硫通入品红溶液中,品红褪色;SO2的漂白具有可逆性,褪色后的溶液加热时又恢复原来的红色.氯气和水反应生成的次氯酸具有漂白性,因而氯气通入品红溶液中也能使品红褪色,次氯酸的漂白不可逆,加热时,不能恢复红色。
故答案为:①品红溶液褪色;②B:褪色的品红又恢复成红色;D:无明显现象。
c.氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应:Cl2+SO2+2H2O=2HCl+H2SO4,生成物都没有漂白性,所以SO2和Cl2按1:1同时通入到品红溶液时,品红溶液并不退色。故答案为:Cl2+SO2+2H2O=2HCl+H2SO4。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】下列关于浓硫酸的叙述,正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物CxHmOn完全燃烧时需要氧气的物质的量是该有机物的x倍,则该有机物分子式中x、m、n的关系不可能是( )
A. x:m:n=1:2:1 B. m:n=2:1 C. m>2x+2 D. m≤2x+2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的恒容密闭容器中,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是
2AB(g)达到平衡的标志是
A. 每断裂1molA-A键,同时也断裂1molB-B键
B. 浓度之比c(A2): c(B2): c(AB)=1:1:2
C. 各物质的浓度不再改变
D. 当混合物的密度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为探究AgNO3溶液和不同类型盐溶液反应的多样性,设计如下实验:

已知:AgSCN为白色难溶物;(SCN)2与卤素单质性质相似,(SCN)2为有色物质。
(1)①中的白色沉淀是___________________。
(2)分离并洗涤①的沉淀,滴加0.5mol/L KI溶液,白色沉淀转变为黄色沉淀,用离子方程式解释上述变化____________________________。
(3)②中可能发生的离子反应有_________________。
(4)实验①的设计目的_______________________。
(5)对于③中红色褪去的原因及Ag+与SCN-反应的情况,小组进行以下分析和设计:
Ⅰ.甲同学认为,红色褪去的原因与平衡移动原理有关,解释为_________________。
Ⅱ.乙同学为了探究③中是否发生Ag+氧化SCN-的反应,又设计以下对比实验:

现象:生成白色沉淀,长时间观察,溶液和沉淀均未发生颜色改变。
Ⅲ.丙同学认为,理论上Ag+能够氧化SCN-,为证明其猜想,设计如下实验:

现象:电流计指针发生偏转,a电极上产生具有金属光泽的物质,b电极附近的溶液发生颜色变化。
丙同学的设计在证明氧化还原反应的优点是___________________________。
(6)通过以上探究,得出AgNO3溶液和不同类型盐溶液反应多样性的结论是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向某恒容的密闭容器中加入1 mol N2和3 mol H2,发生反应:N2(g)+ 3H2(g)![]() 2NH3(g)。此反应达到平衡的标志是( )
2NH3(g)。此反应达到平衡的标志是( )
A. N2、H2和NH3三者共存 B. 容器内气体的浓度不再发生变化
C. N2、H2和NH3的物质的量浓度相等 D. 单位时间消耗0.1molN2的同时生成0.2 mol NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A→C分两步进行:①A→B,②B→C。反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能)。下列说法正确的是
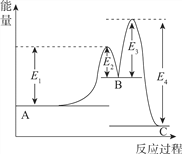
A. 两步反应的ΔH均大于0 B. 加入催化剂能改变反应的焓变
C. 三种物质中C最稳定 D. A→C反应的ΔH=E4-E1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com