
(13分)Ⅰ.(1)反应I2+2S2O32—=2I—+S4O62—常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择______(填序号)。
①1mL 0.01 mol?L—1的碘水 ②1mL 0.001 mol?L—1的碘水
③4mL 0.01 mol?L—1的Na2S2O3溶液 ④4mL 0.001 mol?L—1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O32—)=_______________。
Ⅱ.合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g) 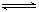 CO2(g)+H2(g) ΔH <0,200℃时,该反应的平衡常数为1/2.25,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol?L—1)变化如下:
CO2(g)+H2(g) ΔH <0,200℃时,该反应的平衡常数为1/2.25,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol?L—1)变化如下:
| | 0min | 5min | 10min |
| CO | 0.01 | | 0.0056 |
| H2O | 0.01 | | 0.0156 |
| CO2 | 0 | | 0.0044 |
| H2 | 0 | | 0.0044 |
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案科目:高中化学 来源: 题型:
(13分)(1)过氧化钠可用作于制氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(2)工业上制取漂白粉的化学方程式为______________ ______。
(3)在标准状况下,33.6 L氯气的质量是________g,将红热的铁丝与其完全反应,反应的化学方程式为 ,最多可消耗铁的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省厦门市翔安一中高一上学期期中考试化学试卷 题型:填空题
(13分)(1)过氧化钠可用作于制氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(2)工业上制取漂白粉的化学方程式为______________ ______。
(3)在标准状况下,33.6 L氯气的质量是________g,将红热的铁丝与其完全反应,反应的化学方程式为 ,最多可消耗铁的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年黑龙江省高三10月月考化学试卷(解析版) 题型:填空题
(13分)Ⅰ.(1)反应I2+2S2O32—=2I—+S4O62—常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择______(填序号)。
①1mL 0.01 mol•L—1的碘水 ②1mL 0.001 mol•L—1的碘水
③4mL 0.01 mol•L—1的Na2S2O3溶液 ④4mL 0.001 mol•L—1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O32—)=_______________。
Ⅱ.合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH <0,200℃时,该反应的平衡常数为1/2.25,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol•L—1)变化如下:
CO2(g)+H2(g) ΔH <0,200℃时,该反应的平衡常数为1/2.25,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol•L—1)变化如下:
|
|
0min |
5min |
10min |
|
CO |
0.01 |
|
0.0056 |
|
H2O |
0.01 |
|
0.0156 |
|
CO2 |
0 |
|
0.0044 |
|
H2 |
0 |
|
0.0044 |
(1) 请分别计算CO、H2O、CO2、H2的平衡浓度__________,_________,________,_______。
(2)CO的平衡转化率为____________,欲提高CO的转化率,下列措施中可行的是_____(填序号)。
a.增加压强 b.降低温度
c.体积不变,再充入CO d.更换催化剂
e.体积不变,再充入0.1molH2O
(3) 若5min~10min只改变了某一条件,该条件是__________,如何改变的___________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省潍坊市高三上学期期末考试化学试卷 题型:填空题
(13分)(1)“天宫一号”于2011年9月在酒泉卫星发射中心发射,标志着我国的航空航天技术迈进了一大步。火箭的第一、二级发动机中,所用的燃料为偏二甲胼和四氧化二氮,偏二甲肼可用胼来制备。
①用肼(N2H4)为燃料,四氧化二氮做氧化剂,两者反应生成氮气和气态水。
已知:N2(g)+2O2(g)=N2O4(g) △H=10.7kJ· mol-1[
N2H4(g)+02(g)=N2(g)+2H20(g) △H=-543 kJ· mol-1
写出气态肼和N2O4反应的热化学方程式为 .
②已知四氧化二氮在大气中或在较高温度下很难稳定存在,它很容易转化为二氧化氮。试推断由二氧化氮制取四氧化二氮的反应条件(或措施): 。
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图l所示装置中,以稀土金属材料做惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y203的Zr02固体,它在高温下能传导阳极生成的02-离子(02+4e →202-)。

①c电极的名称为 ,d电极上的电极反应式为 。
②如图2所示电解l00mL0.5 mol·L-1CuS04溶液,a电极上的电极反应式为
。若a电极产生56mL(标准状况)气体,则所得溶液的pH= (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入 (填序号)。
a. CuO b. Cu(OH)2 c.CuC03 d.Cu2(OH)2C03
查看答案和解析>>
科目:高中化学 来源:2014届福建省厦门市高一上学期期中考试化学试卷 题型:填空题
(13分)(1)过氧化钠可用作于制氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(2)工业上制取漂白粉的化学方程式为______________ ______。
(3)在标准状况下,33.6 L氯气的质量是________g,将红热的铁丝与其完全反应,反应的化学方程式为 ,最多可消耗铁的物质的量为 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com