
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)可表示为( )
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)可表示为( )
A. v(NH3)=0.010mol/(L·s) B. v(O2)=0.0010mol/(L·s)
C. v(NO)=0.0010 mol/(L·s) D. v(H2O)=0.45 mol/(L·s)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2 mol水的摩尔质量和1 mol水的摩尔质量
B.200 mL 1 mol/L氯化钙溶液中c(Cl﹣)和100 mL 2 mol/L氯化钾溶液中c(Cl﹣)
C.64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示: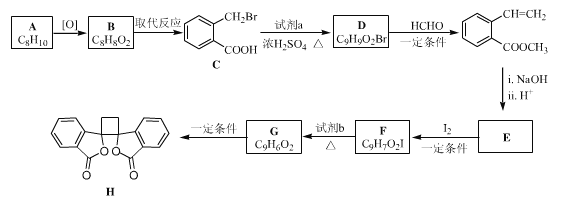
已知:
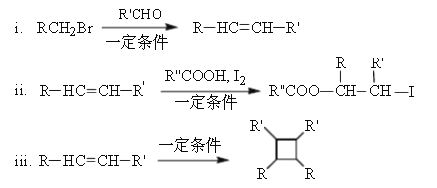
(以上R、R’、R’’代表氢、或烃基等)
(1)a属于芳香烃,名称是______________,B生成C的反应类型是__________。
(2)试剂a是(写结构简式)____________,HCHO的电子式是________________。
(3)E的结构简式是____________。
(4)由F生成G的化学方程式是 _________。
(5)二取代芳香化合物W是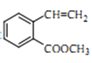 的同分异构体,能使溴的四氯化碳溶液褪色,能犮生银镜反应,能发生水解反应,W共有_______种(不含顺反异构和其他立体异构)。其中核磁共振氢谱为五组峰的结构简式为___________。
的同分异构体,能使溴的四氯化碳溶液褪色,能犮生银镜反应,能发生水解反应,W共有_______种(不含顺反异构和其他立体异构)。其中核磁共振氢谱为五组峰的结构简式为___________。
(6)以乙醇为起始原料,结合己知信息选用必要的无机试剂合成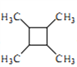 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。________________
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。B是红棕色固体,D是红棕色气体,E是常见的无色液体,G是淡黄色粉末。
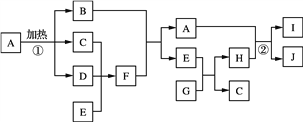
(1)F的化学式为__________。
(2)E的电子式为__________。
(3)写出E+G→H+C的化学方程式______________。
(4)写出反应②的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中有着重要的应用。下列叙述错误的是( )
A.燃煤中加入生石灰可以减少酸雨的形成
B.高纯度的二氧化硅广泛用于制作光导纤维
C.花生油中的主要成分属于酯类,是天然高分子化合物
D.碳纳米管表面积大,可用作新型储氢材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A. 等物质的量的硫蒸气和固体硫分别完全燃烧,前者放出热量多
B. 由C(石墨)=C(金刚石) △H =+1.90 kJ/mol可知,金刚石比石墨稳定
C. 在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l) △H=-285.8kJ/mol
D. 2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0 反应为熵增反应,任何温度下能自发进行
4NO2(g)+O2(g) ΔH>0 反应为熵增反应,任何温度下能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关“生物界和非生物界具有统一性”的说法正确的是
A. 具体表现为在无机自然界含有的元素在生物体内均可以找到
B. 具体表现为在细胞内各种元素的含量和无机自然界相同
C. 这种现象的表现之一是细胞中的氧元素的含量与非生物界中一样,都是含量最高的元素
D. 这种现象产生的原因与细胞膜的功能特点有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是( )
A. Ag+、K+、NO3-、Cl- B. K+、Na+、Cl-、SO42-
C. Ca2+、Mg2+、OH-、Cl- D. H+、Na+、CO32-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。
Ⅰ.测定化学反应速率
该同学利用如图装置测定反应速率(药品:稀硫酸、Na2S2O3溶液等)。

(1)除如图装置所示的实验用品外,还需要的一件实验仪器用品是________________;请写出在圆底烧瓶中所发生反应的离子方程式为___________________________________________。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是____________________________________。
(3)利用该化学反应,试简述测定反应速率的其他方法:___________________(写一种)。
Ⅱ.探究化学反应速率的影响因素
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。
(已知 I2+2 Na2S2O3= Na2S4O6+2 NaI,其中Na2S2O3溶液均足量)
实验序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | T1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | T2 |
③ | 6.0 | 2.0 | 4.0 | Vx | T3 |
(4)表中Vx=__________mL,该实验中加入淀粉的目的为_______________________;请判断T1、T2、T3的大小关系,并总结实验所得出的结论__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com