
| 4.66g |
| 233g/mol |
| 2.24L |
| 22.4L/mol |
| 1 |
| 3 |
| 45.3g-0.1mol×(27+18)g/mol-0.2mol×96g/mol |
| 18g/mol |
| 45.3g |
| 453g/mol |
| 2 |
| 3 |
| 1 |
| 2 |
| 2 |
| 3 |


 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
| A、O2+2H2O+4e-=4OH- |
| B、2H++2e=H2↑ |
| C、4 OH-=2H2O+O2+4e- |
| D、Fe=Fe2++2e- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| CH2(COOC2H5)2 |
| C2H5OH |
| ①OH-,②H3O+ |
| ③△ |
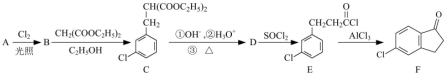
查看答案和解析>>
科目:高中化学 来源: 题型:
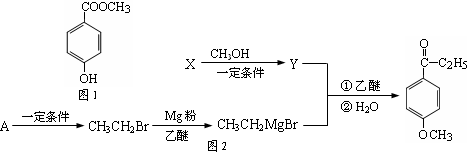
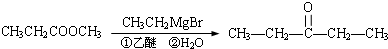
查看答案和解析>>
科目:高中化学 来源: 题型:
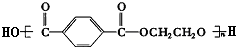
查看答案和解析>>
科目:高中化学 来源: 题型:
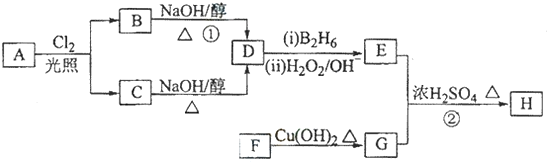

查看答案和解析>>
科目:高中化学 来源: 题型:
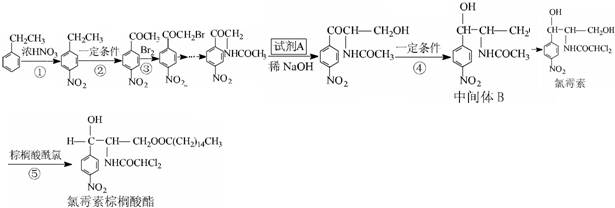


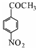 的同分异构体甚多,其中含有-NO2、-CHO、-CH3、
的同分异构体甚多,其中含有-NO2、-CHO、-CH3、 四种基团的同分异构体共有6种,结构简式为
四种基团的同分异构体共有6种,结构简式为 、
、查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主要成分是碱式碳酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;无 |
| B | 铜表面易形成致密的氧化膜 | 铜制容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 向硫酸铜溶液通入氨气,有深蓝色沉淀产生,过滤后灼烧滤渣,最后变成黑色固体 | 把铜丝放在酒精灯火焰上灼烧,铜丝表面变黑 | Ⅰ对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com