
��12�֣�����β���ﺬ��NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�N2(g) + O2(g)  2NO(g) ��H > 0��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
2NO(g) ��H > 0��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
��1��ij�¶��£���2L���ܱ������г���N2��O2��1mol,5���Ӻ�O2�����ʵ���Ϊ0.5 mol����N2�ķ�Ӧ���� ��
��2���ٶ��÷�Ӧ���ں��������½��У��жϸ÷�Ӧ�ﵽƽ��ı�־ ��
A.����1molN2ͬʱ����1molO2 B.��������ܶȲ���
C.�������ƽ����Է����������� D.2V(N2)��=V(NO)��
��3����N2��O2�Ļ�����������º����ܱ������У����б仯������ȷ���� ������ĸ��ţ���

��4������º��ݵ��ܱ������г�������ʵ�����N2��O2���ﵽƽ��״̬���������г���һ����NO�����´ﵽ��ѧƽ��״̬����ԭƽ��״̬��ȣ���ʱƽ��������NO��������� ����������С�����䡱��
��5�����¶��£�ijʱ�̲��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10-1mol/L��4.0��10-2mol/L��3.0��10-3mol/L����ʱ��Ӧ ������ڻ�ѧƽ��״̬������������Ӧ������С������淴Ӧ������С�����������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 2NO��g����H��0
2NO��g����H��0| c2(NO) |
| c(N2)?c(O2) |
| c2(NO) |
| c(N2)?c(O2) |
| (3��10-3 )2 |
| (2.5��10-1)��(4.0��10-2) |
| (3��10-3 )2 |
| (2.5��10-1)��(4.0��10-2) |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�콭��ʡ��ɫ��У������һ��������ѧ�Ծ� ���ͣ������
��12�֣�����β���ﺬ��NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�N2(g) + O2(g)  2NO(g) ��H > 0��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
2NO(g) ��H > 0��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
��1��ij�¶��£���2L���ܱ������г���N2��O2��1mol,5���Ӻ�O2�����ʵ���Ϊ0.5 mol����N2�ķ�Ӧ���� ��
��2���ٶ��÷�Ӧ���ں��������½��У��жϸ÷�Ӧ�ﵽƽ��ı�־ ��
| A������1molN2ͬʱ����1molO2 | B����������ܶȲ��� |
| C���������ƽ����Է����������� | D��2V(N2)��=V(NO)�� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013������ʡ��������˫��ѧУ���������ģ�⻯ѧ�Ծ����������� ���ͣ������
����β���ﺬ��NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�
N2(g) + O2(g)  2NO(g) ��H > 0
2NO(g) ��H > 0
��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
��1���÷�Ӧ��ƽ�ⳣ������ʽΪ
��2�����¶��£���2L�ܱ������г���N2��O2��1mol��ƽ��ʱ��N2��ת������ %��������������
��3�����¶��£�ijʱ�̲��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10-1mol/L��4.0��10-2mol/L ��3.0��10-3mol/L����ʱ��Ӧ (����ڻ�ѧƽ��״̬������������Ӧ������С������淴Ӧ������С����������� .
��4����N2��O2�Ļ�����������º����ܱ������У����б仯������ȷ���� ������ĸ��ţ���
��5������º��ݵ��ܱ������г�������ʵ�����N2��O2���ﵽƽ��״̬���������г���һ����NO�����´ﵽ��ѧƽ��״̬����ԭƽ��״̬��ȣ���ʱƽ��������NO��������� ��������С�����䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ������ʡ���������ģ�⻯ѧ�Ծ��������棩 ���ͣ������
����β���ﺬ��NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�
N2(g) + O2(g)  2NO(g) ��H > 0
2NO(g) ��H > 0
��֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K=64��10-4����ش�
��1���÷�Ӧ��ƽ�ⳣ������ʽΪ
��2�����¶��£���2L�ܱ������г���N2��O2��1mol��ƽ��ʱ��N2��ת������ %��������������
��3�����¶��£�ijʱ�̲��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10-1mol/L��4.0��10-2mol/L ��3.0��10-3mol/L����ʱ��Ӧ (����ڻ�ѧƽ��״̬������������Ӧ������С������淴Ӧ������С����������� .
��4����N2��O2�Ļ�����������º����ܱ������У����б仯������ȷ���� ������ĸ��ţ���
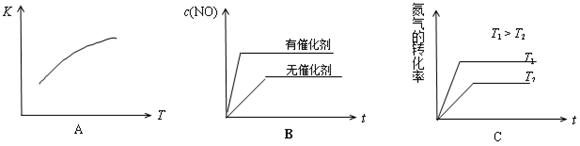
��5������º��ݵ��ܱ������г�������ʵ�����N2��O2���ﵽƽ��״̬���������г���һ����NO�����´ﵽ��ѧƽ��״̬����ԭƽ��״̬��ȣ���ʱƽ��������NO��������� ��������С�����䣩
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com