
【题目】电离方程式错误的是
A. CaCl2=Ca2++2Cl- B. NaHSO4=Na++H++SO42-
C. HNO3=H++NO3- D. KClO3=K++Cl-+3O2-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有一种天然黄铜矿主要成分为CuFeS2 (含SiO2),为了测定该黄铜矿的纯度,某同学设计了如图1实验:

称取研细的黄铜矿样品1.150g煅烧,生成Cu、Fe2O3 、FeO和SO2气体,实验后取d中溶液的1/5置于锥形瓶中,用0.01mo1/L标准碘溶液进行滴定,初读数为0.10mL,末读数如图2所示.完成下列填空:
(1)装置c的作用是____________________________。
(2)上述反应结束后,仍需通一段时间的空气,其目的是_____________________。
(3)滴定时,标准碘溶液所耗体积为_____mL;用化学方程式表示滴定的原理:________________________________________。
(4)计算该黄铜矿的纯度___________________。
(5)工业上利用黄铜矿冶炼铜产生的炉渣(含Fe2O3 、FeO、SiO2、Al2O3)可制备Fe2O3.
选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液
所选试剂为_________;证明炉渣中含有FeO的实验现象为:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用盐酸的标准溶液滴定待测氢氧化钠的浓度时,用甲基橙作指示剂,达到滴定终点时,溶液的颜色变化是( )
A.由红色变为橙色B.由无色变为浅红色
C.由黄色变为橙色D.由红色变为浅红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存于同一水溶液中的是
A. HCO3- 、Na+、K+、H+ B. NO3-、Cl-、Na+、Ag+
C. Mg2+、K+、NO3-、OH- D. Cu2+、H+、Na+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对应化学反应的离子方程式中正确的是
A. 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B. 向NaAlO2溶液中通入过量的CO2:AlO2-+4CO2+2H2O=Al3++4HCO3-
C. 过量的铁和稀硝酸反应:3Fe + 2NO3-+ 8H+= 3Fe2++ 2NO↑+ 4H2O
D. NH4HCO3溶液与足量 NaOH 溶液混合:HCO3-+OH- =CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯甲酸酯类是一类局部麻醉药,化合物M是该类药物之一。合成M的一种路线如下:
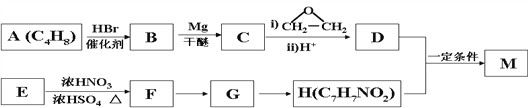
已知以下信息:
①核磁共振氢谱显示B只有一种化学环境的氢,H苯环上有两种化学环境的氢。
②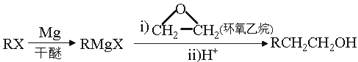 。
。
③E为芳香烃,其相对分子质量为92。④![]() (苯胺,易被氧化)。
(苯胺,易被氧化)。
回答下列问题:
(1)A的结构简式为_________________,其化学名称是__________。
(2)由E生成F的化学方程式为__________________。
(3)由G生成H的反应类型为__________________。
(4)M的结构简式为________________________________。
(5)D的同分异构体中不能与金属钠反应生成氢气的共有_________种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为6:1的是_________________。
(6)参照上述合成路线,以乙烯和环氧乙烷为原料(无机试剂任选)制备1,6-己二醛,设计合成路线 ___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A,B,C,D是同周期或同主族的相邻元素: ![]()
(1)已知:A元素的最低价为﹣3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子的质量数为 .
(2)写出元素符号A , C , D .
(3)A,B,C三种元素最高价氧化物的水化物中酸性最强的是 . (填化学式)
(4)B,D两种元素和氢组成的气态氢化物中稳定性强的是 , 还原性最强的是(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源。
(1)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。已知:
①H2(g)+Cl2(g)=2HCl(g) ΔH=-a ![]()
②E(H-H)=b![]() , E(Cl-Cl)=c
, E(Cl-Cl)=c ![]()
则:E(H-Cl)=_____________kJ·mol-1。
(2)实验中不能直接测出由石墨和氢气反应生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧反应的反应热,求由石墨生成甲烷的反应热。已知:
①CH4(g)+2O2(g)==CO2(g)+2H2O(l) △H=-a kJ·mol-1
②C(石墨)+O2(g)==CO2(g) △H=-b kJ·mol-1
③H2(g)+1/2O2(g)==H2O(l) △H=-c kJ·mol-1
则反应C(石墨)+2H2(g) → CH4(g)的反应热△H=________kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com