
已知气体的密度与它的摩尔质量成正比。一只气球若放在空气(空气的平均摩尔质量是29 g·mol-1)中可静止不动,那么在相同条件下该气球放在下列气体中会下沉的是
A.O2 B.Cl2 C.CO2 D.CH4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年广东省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列各组离子,能在指定溶液中大量共存的是
A.无色溶液中:Na+、SO42-、CO32-、Cl-
B.能使紫色石蕊试剂变红的溶液中:OH-、K+、Ba2+、Na+
C.透明的酸性溶液中:Fe3+、Mg2+、Cl-、NO3-
D.碱性溶液中:NH4+、Ba2+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期月考(三)化学试卷(解析版) 题型:选择题
设NA代表阿伏伽德罗常数的数值,则下列说法正确的是( )
A.常温常压下,1mol氦气含有的核外电子数为4NA
B.0.25mol Na2O2中含有的阴离子数为0.5NA
C.50ml 18.4mol/L浓硫酸与足量铜微热,生成气体0.46NA
D.25℃时,7g C2H4和C3H6的混合气体中,含有NA个C—H键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期期中测试化学试卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行如下可逆反应X(g)+Y(g)  Z(g)+W(s) ΔH>0。下列叙述中,正确的是:
Z(g)+W(s) ΔH>0。下列叙述中,正确的是:
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.改变条件,又达新平衡,此时上述反应的平衡常数K值一定增大
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三12月月考化学试卷(解析版) 题型:选择题
下列有关结构和性质的说法中,正确的是 ( )
A.Si、P、S、 Cl元素的单质与氢气化合越来越剧烈
B.元素原子的最外层电子数越多,元素的金属性越强
C.第三周期主族元素从左到右的最高价含氧酸酸性减弱
D.元素中期表共有18列,第8列属于第ⅧB族、第17列属于第ⅫA族
查看答案和解析>>
科目:高中化学 来源:2016届山东省济宁市高三上学期期中考试化学试卷(解析版) 题型:选择题
以下离子检验正确的是( )
A.检验试液中的SO42-:试液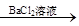 白色沉淀
白色沉淀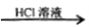 白色沉淀
白色沉淀
B.检验试液中的Cl-:试液 无沉淀
无沉淀 白色沉淀
白色沉淀
C.检验试液中的Fe2+:试液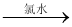 无明显现象
无明显现象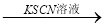 血红色溶液
血红色溶液
D.检验试液中的NH4+ :试液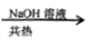 气体逸出
气体逸出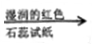 试纸变蓝
试纸变蓝
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列有关金属腐蚀与防护的说法正确的是
A.钢柱在水下部分比在空气与水交界处更容易腐蚀
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高一上学期期中测试化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,11.2L氧气所含的原子数为NA
B.1.8g的NH4+离子中含有的电子数为11NA
C.常温常压下,48gO3含有的氧原子数为3NA
D.5.6g金属铁与足量稀盐酸反应时失去的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:填空题
硼镁泥主要成份是MgO(占35%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质。从硼镁泥中提取MgSO4·7H2O的流程如下:
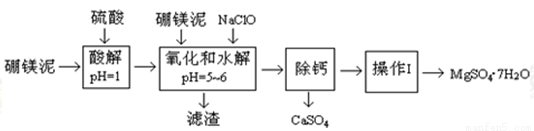
已知:NaClO与Mn2+反应产生MnO2沉淀.
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
开始沉淀pH | 2.3 | 4.0 | 7.6 |
完全沉淀pH | 4.1 | 5.2 | 9.6 |
根据题意回答第(1)~(5)题:
(1)在酸解过程中,欲加快酸解时的化学反应速率,请提出两种可行的措施: 、 。
(2)加入的NaClO可与Mn2+反应:Mn2+ + ClO- + H2O = MnO2↓ + 2H+ + Cl-,还有一种离子也会被NaClO氧化,并发生水解,该反应的离子方程式为 。
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3 、MnO2外,还有 。
(4)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤是蒸发浓缩, 。“操作I”是将滤液继续蒸发浓缩,冷却结晶, __________ ,便得到了MgSO4·7H2O。
(5)实验中提供的硼镁泥共100 g,得到的MgSO4·7H2O为172.2 g,计算MgSO4·7H2O的产率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com