
【题目】若用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.22.4 L NH3中含氮原子数为 NA
B.1 mol Na2O2与水完全反应时转移的电子数为NA
C.100 mL 2.0 molL﹣1 NH4HCO3溶液中NH4+数为0.2NA
D.1 mol O2和2 mol SO2在密闭容器中充分反应后的分子数等于2NA
科目:高中化学 来源: 题型:
【题目】人类的生产生活离不开金属材料,金属及金属材料在生产、生活中应用广泛.
(1)生活中常用的铁锅炒菜,主要是利用了铁的;铁在潮湿的空气中容易锈蚀,喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝 , 喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,写出其中涉及到的一个化学方程式: .
(2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
①A、B、C三种金属的活动性顺序为 .
②金属C是 , 已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究 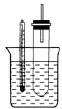
实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL溴乙烷,振荡.
实验操作Ⅱ:将试管如图固定后,水浴加热.
(1)水浴加热的优点是 .
(2)试管口安装一长导管的作用是 .
(3)了解生成物中乙醇的相对分子质量可用的谱图是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求准确表达下列变化过程中的化学用语,其中(1)~(3)写化学方程式,(4)~(5)写离子方程式.
(1)铁丝在氯气中燃烧;
(2)能体现SO2氧化性;
(3)镁在二氧化碳中燃烧;
(4)NaOH溶液与NaHCO3溶液反应;
(5)用氯化铁溶液刻画电路板 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO,CH4均为常见的可燃气体.
(1)等体积的CO,CH4在相同的条件下分别完全燃烧,转移的电子数之比为 .
(2)120℃,101kPa下,a mL由CO,CH4组成的混合气体在b mL氧气中完全燃烧后,恢复至原来的温度与压强.
①若混合气体与氧气恰好完全反应,产生b mLCO2 , 则混合气体中CH4的体积分数为%.
②若燃烧后气体体积缩小了 ![]() mL,则a与b的关系为(数学表达式表示).
mL,则a与b的关系为(数学表达式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~J均为有机化合物.
根据图中信息,回答下列问题:
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.20%.B的一氯代物仅有一种,B的结构简式为 .
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为 .
(3)由A生成D的反应类型是 .
(4)G的分子式为C6H10O4 , 0.146gG需用20mL 0.100molL﹣1 NaOH溶液完全中和,J是一种高分子化合物.则由G转化为J的化学方程式为 .
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如图反应:,则由E和A反应生成F的化学方程式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是人类文明发展的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)工业生产粗硅的反应有:SiO2+2C![]() Si(粗)+2CO↑,SiO2+3C
Si(粗)+2CO↑,SiO2+3C![]() SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
(2)工业上可以通过如下图所示的流程制取纯硅:

①若反应I为 Si(粗)+3HCl![]() SiHCl3+H2,则反应II的化学方程式为 。
SiHCl3+H2,则反应II的化学方程式为 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另 一种物质,写出该反应的化学方程式: 。
③设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com