
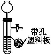
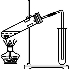
下列制备气体的实验设计中错误的是( )
选项ABCD
药品NH4Cl
与Ca(OH)2石灰石和
稀盐酸稀硝酸
和铜片KMnO4
与浓盐酸
装置

科目:高中化学 来源:2014高考化学名师知识点精编 专题7元素周期表与元素周期律练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D.第三周期元素的离子半径从左到右逐渐减小
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题3离子反应练习卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.向40 mL 8 mol/L的硝酸溶液中加入5.6 g铁粉:Fe+4H++NO3— Fe3++NO↑+2H2O
Fe3++NO↑+2H2O
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO- CaSO3↓+2HClO
CaSO3↓+2HClO
C.漂白粉溶液在空气中失效:ClO-+CO2+H2O HClO+HCO3—
HClO+HCO3—
D.Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO42— BaSO4↓+2H2O
BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题2化学计量及其应用练习卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列有关NA 的叙述中正确的有( )
①标准状况下,20 g重水(D2O)中含有的电子数为10NA
②0.5 mol Fe2+与足量的H2O2溶液反应,转移NA个电子
③将2 mol NO和1 mol O2混合后,体系中的分子总数为3NA
④常温下,0.4 mol SiO2所含的共价键数目为1.6NA
⑤2 mol·L-1碳酸钠溶液中Na+的数目是2NA
⑥1 mol氯气溶解在水中得到的新制氯水中氢离子的数目是NA
⑦22.4 L的N2的共用电子对数为3NA
A.2个B.3个C.4个D.5个
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题23实验方案的设计与评价练习卷(解析版) 题型:选择题
下列实验装置不能达到实验目的的是( )
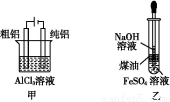
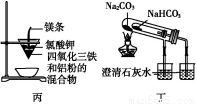
A.甲装置电解精炼铝
B.乙装置制备Fe(OH)2
C.丙装置可得到金属铁
D.丁装置验证NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题22物质的检验、分离和提纯练习卷(解析版) 题型:选择题
实验是研究化学的基础,下列有关实验的方法、装置或操作都正确的是( )
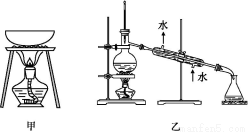
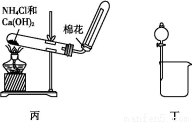
A.从KI和I2的固体混合物中回收I2,可使用如图甲所示实验装置
B.分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置
C.实验室制氨气,如图丙所示
D.分离乙醇和乙酸的混合液,实验装置如图丁所示
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题21化学实验基础练习卷(解析版) 题型:实验题
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中Na2CO3的质量分数。
【方案一】 称取一定质量的固体样品,通过加热至恒重后冷却,称量剩余固体质量,计算。
(1)下列仪器中,在灼烧固体样品时必须用到的是 (填名称)。

(2)实验中需加热至恒重的目的是: 。
(3)实验中确定加热至恒重的方法是: 。
(4)若加热过程中有晶体迸溅出来,则测得的结果 (填“偏大”、“偏小”或“不变”)。
【方案二】 称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤,干燥沉淀,称量固体质量,计算。
(已知:Ba2++OH-+HC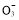
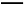 BaCO3↓+H2O)
BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为 。
(2)实验中判断沉淀是否完全的方法是 。
(3)实验中洗涤沉淀的操作是 。
(4)实验中判断沉淀是否洗涤干净的方法是 。
【方案三】 按如图所示装置进行实验:

(1)B装置内所盛试剂是 ;D装置的作用是 ;分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.9 g样品,实验后测得C装置增重8.8 g,则样品中Na2CO3的质量分数为 。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题20同分异构反应类型有机合成练习卷(解析版) 题型:填空题
扑热息痛(学名对乙酰氨基酚)是生活中常用到的一种解热镇痛药。以苯为原料合成扑热息痛的部分转化如下: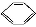
 A
A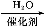 B
B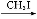 C
C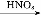
 →…→D
→…→D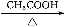
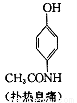
请回答下列问题:
(1)B→C的反应类型为 ,D中官能团的名称为 。
(2)C的结构简式为 。
(3)1 mol 扑热息痛与足量NaOH溶液反应,理论上消耗NaOH的物质的量为 mol。
(4)实验证明B能够与溴水反应,试写出其反应的化学方程式: 。
(5)扑热息痛有多种同分异构体,同时符合下列要求的同分异构体有 种。
①苯环上有两个对位取代基 ②属于氨基酸
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题17氮及其化合物练习卷(解析版) 题型:选择题
物质的量之比为1∶3的锌与稀硝酸混合,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,下列说法中正确的是( )
A.在此反应中硝酸体现强氧化性,全部被还原
B.向反应后的溶液中再加入金属铁,不再发生化学反应
C.该反应中被还原的硝酸与未被还原的硝酸之比为1∶4
D.该反应中被还原的硝酸与未被还原的硝酸之比为1∶5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com